近日,东曜药业黄鹏博士做客写意直播间,与普方生物刘海东博士、博瑞医药黄仰青博士共同探讨《ADC药物研发的挑战和策略》。在此,我们将分享黄鹏博士在直播中阐述的内容。
01
ADC相关的研究背景
抗体偶联药物(ADC)作为“魔术子弹”最典型的应用方式,经过一百多年的研发和技术迭代,最终实现了概念验证,特别是在近三四年内,已有数个ADC药物连续获批,充分证明“魔术子弹”的概念真正走到了现实世界中。近几年,关于ADC的交易和并购金额都非常庞大,可见ADC市场的火热程度,随之也有越来越多的创新药企投入到ADC研发热潮中。ADC药物是大分子抗体药物和小分子化学药物的结合,兼具复杂性和多样性,其研发、生产及质量控制等方面均面临挑战。
02
ADC偶联开发的挑战和策略
ADC相较于传统的化学治疗药物,其优势在于治疗窗口。正是由于ADC具有靶向单抗,得以实现靶向治疗。同时因为靶向性,可以采取活性或者是肿瘤细胞毒性非常强的小分子,作为Payload,组合进行应用,使得ADC的治疗窗口非常大。
依照治疗窗口的大小,可将ADC的研发历程分为数个代次。以最早的随机偶联为第一代,其工艺或Linker尚处于不成熟阶段;后以T-DM1为代表,以实体瘤靶向的ADC-Kadcyla获批上市开始,真正把ADC做成了药物,至此Kadcyla被认为是第二代ADC技术;此后,ADC研发有了整体均一性、亲水性的增强,以及整体ADC分子的稳定性提升等诸多方面的质量改进,均可划为第三代或者是下一代ADC技术,其关键变化实际上是治疗窗口的进一步增大。

针对不同的偶联技术,下一代ADC可以分为两大类,分别是基于天然抗体进行的ADC分子设计,以及基于工程化改造抗体。其中,基于天然的抗体,也可以设计构建均一化或者是定点偶联的ADC。天然抗体中常见的偶联位点包括链间二硫键、IgG抗体保守的N糖基化位点、具有活性反应侧链的赖氨酸等,均可用于定点偶联或是均一化ADC偶联位点的设计。如半胱氨酸可以形成二硫键桥接,连满DAR8,通过不同的工艺优化,可以实现轻重链间的二硫键的偶联。针对赖氨酸,也可以通过亲和肽,或可逆反应的巧妙设计来进行设计,如linchpins分子结构,通常需要考虑整体溶剂可接触表面的情况,以及pKa的具体微环境变化,来设计定点偶联的方式。针对其他氨基酸残基,同样可以做一些定点偶联的设计。
此外,可以对抗体进行工程化改造。基于工程化改造的抗体,也有相应定点偶联的ADC技术涌现。如通过定点突变的半胱氨酸或非天然氨基酸,插入一段特定酶可识别的底物序列,均可实现定点偶联,解决更加均一化的ADC产物的设计问题。
针对均一化和定点偶联的ADC技术,有一些典型工艺路线,通常拿到抗体会进行一些相应的修饰或者是功能化的激活。接下来通常会配合一些可选的Buffer change或者是纯化的步骤,然后进行偶联和后续的纯化工艺。不同的偶联方式,会对应不同的工艺流程。
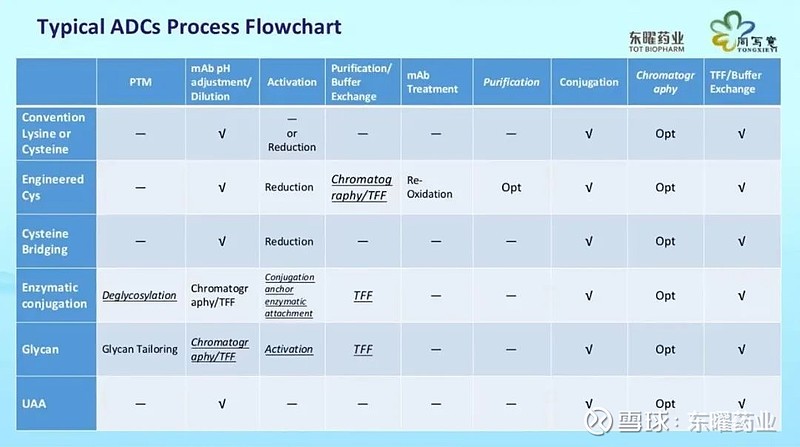
在ADC工艺开发的过程中,面临诸多挑战。例如要考虑抗体对有机溶剂的耐受性与小分子的稳定性,在反应过程中,还要考虑整体反应温度、反应时间,以及杂质的去除等。
在ADC药品的生命周期中,工艺开发一直存在。从最初为非临床与早期临床样品的制备,到晚期临床需要的更大规模的生产,以及后续工艺表征与工艺验证以实现真正的商业化生产,工艺开发伴随着ADC生命周期的不同阶段,会有不同规模的对应需求。
工艺开发也要紧紧围绕着相应的关键质量属性去开展。建立起工艺和质量之间的相关性,才会真正地对药物的药学研究有深刻的理解。
ADC结构复杂,ADC质量相关的表征研究也十分复杂,需要应用多种生物物理或生物化学的分析技术。从另一角度来看,ADC分子结构复杂(包含单抗、Linker和小分子Payload),工艺流程长(包括单抗原液生产、ADC的偶联和制剂生产),所以从供应链的角度来评测,ADC的供应链长且复杂。如果在同一场地或者是集中一地完成ADC研发与生产全流程,可以提升效率,降低管理风险。
03
TAA013案例分享
TAA013是一种靶向Her2偶联DM1的ADC,由东曜药业自主研发。TAA013的单抗、ADC偶联和制剂的研发生产,均在东曜一体化和一站式平台完成。
在具体的工艺开发过程中,我们选择了两步法偶联工艺。首先将 SMCC Linker与曲妥珠单抗偶联;之后偶联上DM1小分子,最终生成T-DM1。
在质量分析过程中,我们发现分子主峰旁多出一个200 Da 左右的“空载Linker”。针对空Linker产生的原因,我们提出两种可能性,一是Linker发生了水解,没有偶联上小分子;二是可能生成了交联副产物。经过深入分析,发现在TAA013的工艺开发中,交联副产物是产生“空载Linker”最主要的原因。针对工艺相关杂质,我们通过还原CE进行相应质量控制。在工艺放大的过程中,我们在小试、中试和商业化规模中,都做到了相应的质量控制,并且进行了不同规模间的相似性比对研究。
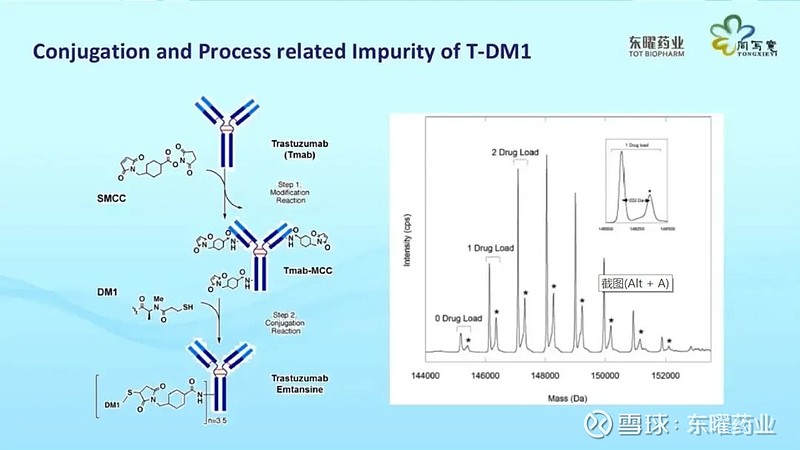
TAA013和Kadcyla的偶联位点是相似的,药物分布也非常相似。这一案例证明,工艺开发和质量分析关系非常紧密,并且在研发过程中能够相互支持验证。
TOT BIOPHARM
东曜药业ADC平台
东曜药业拥有领先的集单抗和抗体偶联药物(ADC)与一体的完整产业平台,我们已建成符合GMP标准的ADC中试及商业化生产车间,配备OEB-5级别隔离器,并布局两台20平米的冻干机,届时产能可达5万瓶/批。
至今,东曜药业已成功助力多个ADC项目顺利开展,包含Ⅰ期和Ⅲ期临床项目,凭借先进的偶联核心技术和ADC分析技术优势、经验证的质量管理体系和符合GMP标准的商业化能力,向合作伙伴提供值得信赖的一站式CDMO服务,赋能ADC药物开发生产。
04
问答环节
Q: 在不同的文献中,还原抗体二硫键使用的剂量不尽相同,有的是5当量,而有的达到了50。请问具体的还原剂用量应该如何把控?
A: 还原剂的用量,取决于工艺的目的是什么,根据目的,进行相应的工艺的开发。具体到还原剂的用量和当量,与整个反应体系以及抗体本身的疏水性都是相关的。实际上不同的抗体,使用同样剂量的还原剂,还原的二硫键的比例往往也不同。所以要针对抗体做有针对性的工艺考察。如果完全还原的话,几十倍甚至是一百倍的当量,都有可能使用。
Q: 在药品研发过程中,如果走到临床部分失败了,而前期投入很多,实际上是很大的浪费。从研发的角度出发,连接子、Payload的选择可以怎样解决这一问题?
A: 药物研发和创新药研发,本身便存在风险,在不同阶段都有失败的可能性。在临床前的阶段,也就是在药物发现的过程中,如果能够做更多深入研究,也就有可能可以降低临床后期失败的风险。
深入理解ADC的作用机制,例如成药性的评估、靶点综合的考虑,能够降低后期失败的风险。但是这仅仅是降低,实际上还要考虑未被满足的临床患者的实际需求,如果有一定的可能性,还是会积极地往后推动,通过临床试验去证明前期的研发设计是否成功。
Q: 请问ADC药物的成药性如何评估?
A:成药性评价,是非常重要的环节,是新药研发、早期发现和后期CMC开发之间的重要桥梁。东曜药业作为一家CDMO公司,能够负责CMC的开发和生产的同时,对于成药性评价,尤其是ADC评价上具有相应的经验。
关于ADC的成药性评价,首先要考虑各自的部分,如大分子抗体部分和小分子部分各自成药性的评价。这两部分相对成熟,具有相应体系化流程的评价方法。针对ADC自身的特殊性,对于偶联药物,需要考虑到偶联后的稳定性、DAR值变化、偶联位点的分布情况等。ADC中常用的小分子具有较强疏水性,偶联后分子整体的亲水性程度是成药性评价的重要一项。可能会影响后续聚体含量的变化、整个PK缩短以及免疫源性的增加,最终导致毒性的增加,所以疏水性、DAR值及分布、Linker的稳定性等,是成药性评价的重要方面。
往期精选
1
东曜药业CDMO | 一站式ADC产业平台 赋能药物开发
2
行业洞见 | ADC是一项综合技术,强强联合创造更大效益
3
东曜药业为您提供一站式创新药CDMO解决方案

关于东曜药业股份有限公司(股票代码:1875.HK)
东曜药业致力于成为全球创新药领域客户的专业合作伙伴。凭借丰富的实践经验和成熟的平台体系,东曜药业与国内外制药公司开展多元的战略合作,提供药物开发生产一站式CDMO解决方案,加速化药、生物药特别是ADC药物的开发和生产,造福广大病患。
Advantages
东曜药业核心优势
符合GMP规范的大规模生物药商业化生产基地,产能充足,采用行业高标准生产设备
ADC一站式产业化平台,具备核心研发技术优势,同时ADC裸抗、原液、制剂等关键生产环节可以在一地集中完成,大幅降低转移成本,减少监管风险
经药监部门审核通过的质量管理体系,贯穿从研发到商业化阶段的全流程
核心团队成熟稳定,拥有生物制药工艺开发、商业化生产、质量、法规申报等领域的丰富行业经验
良好的企业声誉和信用记录,获得业界信赖与认可