SHENGPU 20230724
摘要: 回顾华大基因在甲基化PCR检测肠癌的三项专利,包括筛选甲基化PCR检测的目标区域;血浆游离DNA中SEPT9、ALX4、SDC2三基因甲基化试剂;粪便样本检测ADHFE1基因、PPP2R5C基因和SDC2基因甲基化状态的试剂盒。肯定华大基因的自主发现创新,思考相关的经验教训,思考聚焦,观察未来的技术变迁。
1专利1 基因甲基化PCR检测的目标区域
筛选甲基化PCR检测的目标区域的方法、试剂盒及应用
1.1 时间:2018.01.22申请专利
1.2 主要内容
申请号:201810059375.3
申请日:2018.01.22
发明名称:筛选甲基化PCR检测的目标区域的方法、试剂盒及应用
摘要:本申请公开了一种筛选甲基化PCR检测的目标区域的方法、试剂盒及应用。本申请的方法包括:
(1)从数据库中获取待分析肿瘤甲基化芯片及对应转录组测序数据;
(2)统计正常组与癌症组的甲基化程度值,筛选不同组别中具有显著差异的甲基化位点;
(3)联合转录组测序表达谱的分析,统计相关系数,筛选负相关位点;
(4)将步骤(3)获取的甲基化候选位点,与披露的相关文献关联,筛选获得文献支持报道多且组间甲基化差异程度大、表达量负相关位点;使用回归算法,获取最佳敏感性、特异性的位点集合,即目标区域。
本申请能灵敏、特异获得甲基化PCR检测的目标区域。
1.3 探针引物设计(完成并公布,略)
1.4 主要成果:获得甲基化检测目标基因(结直肠癌与肺癌)
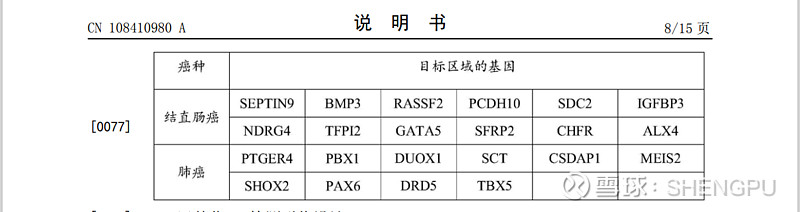
1.5 试剂盒的定型
(未进行)
2 专利2: 血液样本三基因甲基化试剂盒
本项是华大基因2018年研发的
华常康0.0 版本(所谓的液体活检,血液检测)
2.1 专利概要
血浆游离DNA中SEPT9、ALX4、SDC2三基因的甲基化试剂盒(肠癌检测)
申请号:202010999774.5
申请日:2020.09.22
申请人:北京华大吉比爱生物技术有限公司
发明名称:一种检测多基因甲基化的试剂盒及其应用
2.2 摘要
本发明提供了一种检测多基因甲基化的试剂盒及其应用。
所述检测多基因甲基化的试剂盒包括:针对SEPT9基因启动子区域甲基化位点的引物对和探针;针对ALX4基因启动子区域甲基化位点的引物对和探针;针对SDC2基因启动子区域甲基化位点的引物对和探针。
本发明采用多基因甲基化联合检测方法,同时检测血浆游离DNA中三个基因的甲基化水平。经筛选优化,本发明首创的多重探针法降落PCR对结直肠癌进行早期筛查表现出良好的灵敏度和特异性,结直肠进展期腺瘤检出率显著提高,且检测结果稳定,重复性好。
2.3 实验与实施
具体实施:本实施例为与中山肿瘤医院合作项目,完成对414例有效检测样本的分析、评估引物探针组合的临床检测结果。164个结直肠癌患者和250个无患病症状志愿者被招募
2.4 试剂检测肠癌效果评价
血浆样本三基因甲基化检测的效果评估
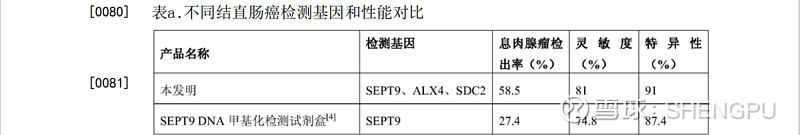
3 专利3:粪便样本的三基因甲基化检测肠癌的专利
3.1 申请日2021.04.23
用于(粪便样本)结直肠癌检测的组合物、试剂盒及应用
摘要:提供了一种用于结直肠癌检测的组合物、试剂盒及应用。
所提供的组合物包含用于检测ADHFE1基因、PPP2R5C基因和SDC2基因甲基化状态的试剂,可以用来检测结直肠癌,具有高的灵敏度和特异性。
3.2 检测的目标基因确定
步骤:首先,发明人对癌症基因组图谱(The Cancer Genome Atlas,TCGA)数据库中的不同基因在肿瘤/非瘤样本的甲基化水平所表现出来的显著性差异进行比较,从而筛选确定了甲基化检测的候选基因:
CDH4、ZNF132、PPP2R5C、LONRF2、ADHFE1、SDC2、NDRG4、BMP3;
利用少量肿瘤/非瘤样本对候选基因进行初步筛选,得到5个候选基因。
比较其在TCGA数据库中的甲基化数据,发现:
相较于BMP3基因和NDRG4基因,ADHFE1、PPP2R5C和SDC2基因均表现为在癌旁组织中的背景更低,在癌组织和癌旁组织也更能表现出更加明显的差异。
3.3 试剂效果评估
实验:共收集了201例结直肠癌样本、184例健康人对照、4例腺瘤样本和7例息肉样本。
合计(396例)
整合三个基因的△Ct值进行分析,AUC可达0.945。最终确定△Ct(ADHFE1)≤8、△Ct(PPP2R5C)≤5、△Ct(SDC2)≤12时判定该基因检测阳性,当任意基因阳性时则判定该样本检测阳性,
在此判定条件下,在特异性为94.02%时,灵敏性可达87.56%。
4 事后回顾
4.1 专利申请延迟于年报相关内容约2年
结论: 从专利申请角度看,应该是基于保密等原因,专利申请迟于实际工作约2年,从论文角度看,未研究。
支持结论的事实如下:
2018年报:临床试验和大规模人群验证后,公司正在努力推进肠癌血液早筛、***以及全外显子基因检测,基于外周血ctDNA的新一代液体活检产品转化,肠癌一站式检测等新产品转产发布。
2019年报:产品第13项:华常康™ 无创肠癌筛查基因检测提取粪便中肠道脱落细胞DNA,用荧光定量PCR技术检测肠癌相关基因基因甲基化水平,分析受检者罹患结直肠肿瘤及癌前病变的风险。
4.2 华大基因在甲基化PCR检测肠癌的技术路径回顾
第一步 筛选甲基化PCR检测的目标区域的方法、试剂盒及应用
第二步 技术路线1:定型:血浆游离DNA中SEPT9、ALX4、SDC2三基因的甲基化试剂盒(肠癌检测)评价:血液检测 灵敏度(可检出)指标81%尚不理想。
第三步 技术路线2:粪便DNA样本,检测ADHFE1基因、PPP2R5C基因和SDC2基因甲基化状态
灵敏度(可检出)指标87.56%可接受状态,但是与竞品比较,系不对称比较,弱。
第四步 粪便DNA甲基化 并联 便隐血 (FIT),2022年末推出 COLOTECT 3.0
按照2022年11月29美国商业资讯BGI启动改进的非侵入性结直肠癌癌症筛查试验,COLOTECT 3.0。
基本数据:检测CRC的灵敏度为96.08%,检测晚期癌前病变(APL)的灵敏度为52.5%,
4.3 思考
从2019年推出华常康到2022年末,用3年时间,并联已有、已知、的传统的FIT,与精密科学的一致。这个针对市场待开发、不成熟的打法?在经营方面,华大基因中期(1-2年内)是否应该战略性聚焦比如:肠癌与质谱?
肯定华大基因的自主发现与创新;
思考相关的经验教训,思考聚焦;
观察未来的技术变迁。