SHENGPU 2023.05.14
概要:在2019年,华大基因的净利润不足3.0亿元,但向美国Natera,Inc.购买ctDNA的技术2.95亿元。结合华大基因自主测序平台,华见微®肿瘤MRD定制化检测产品于2020年9月正式发布。需要适当回顾此事件,并连同事件2:用华大因源与华大数极的股权融资5.9亿;事件3:两次7亿元的股权激励行为一并纳入历史视野观察。
1 华大基因的ctDNA技术获取
1.1 Natera公司的Signatera技术
不同于临床常用的固定panel检测,采用定制化的panel来进行监测。是美国Natera公司在肿瘤复发监测领域开发的一项新技术,该技术通过全外显子组测序和独有的克隆演化算法分析挑选适合每一位患者的突变特征,为每位患者提供量身定制的高灵敏性的ctDNA监测,可用于评估患者的治疗效果、早期发现复发风险等,更精准更早地预测肿瘤复发和进展。
1.2华大基因的一个产品
2019年购买专利技术,结合华大基因自主测序平台,华见微® 肿瘤MRD定制化检测产品于2020年9月CSCO卫星会上正式发布。
华见微® 肿瘤MRD概要:对肿瘤组织进行全外显子测序,基于其测序结果,为患者设计定制化位点检测;在监测时采集外周血并检测ctDNA(循环肿瘤DNA),对患者的微小残留病灶(MRD)进行监测,记录肿瘤分子含量和变化趋势,为临床医生早期发现患者复发和及时判断疗效提供参考依据。
1.3 华大基因2019向美国Natera,Inc.购买技术与合作的概要
华大基因获取此技术的购买对价:2.95亿元人民币。其中2019年度支付:263,446,084.03元,2022年度支付:31,340,700.00元;合计:2.95亿元。
2019年财报注:预付专利款系公司向美国Natera,Inc.(以下简称“Natera公司”)购买肿瘤基因检测技术及生育健康基因检测技术的十年使用权,并将该技术相关的产品商业化,该专利使用权合同总金额约5,000.00万美金。
2022年度追加约450万美金。
1.4 此项技术的账面净值(2022年末)为1.10亿元
按照各年财报核算以计提减值准备情况,财务核算分两个科目处理:其他非流动资产及无形资产。2020-2022合计减值(含资产减值损失,无形资产摊销,其他长期非流动资产计入成本等)约:1.85亿元。
表01:其他非流动资产-预付专利款
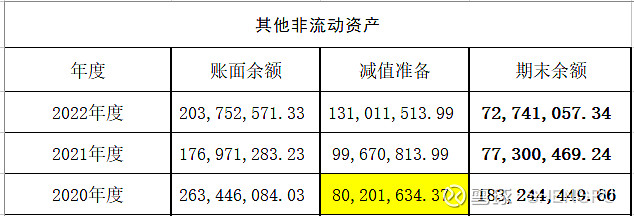
表02:无形资产-非专利技术

说明:1计提摊销是估计,2、表中个别数据可能与报表的减值准备数据有1200万左右差异,不排除有可能是2021年度的报表错误。
但本文不讨论这些无太多意义的事项。
2 华大基因购买后的后续工作
2.1 后续工作
基于华大基因的国产自主测序平台,对该技术进行了拓展和优化。
非常明显Natera公司的Signatera技术以前是基于ILMN的测序仪,华大基因需要使用到MGI的测序仪上。
技术适用范围拓展到常见肿瘤,而非某一种,具体见华大基因年报产品列示。
技术适用范围拓展到用药指导、微小残留病灶评估、复发监测
2.2市场一些宣传
金域医学(2022.05.12)宣称: 可达到检测灵敏度2/万.
华大基因(2020.09.25): 最低检测限(LOD):1/万
详情请阅
文献01 华见微®肿瘤MRD定制化检测
文献02:
金域医学打造“惠民3000”肿瘤检测体系,让基因检测可负担、更可及 (qq.com)
2.3 2020年以来的市场监管背景
对于液体活检与高通量测序的肿瘤检测产品:
2020年,同时采用高通量测序技术和液体活检技术的泛肿瘤基因检测产品获得FDA批准上市,标志着液体活检技术临床应用已获得监管机构及行业认可。
美国NCCN结直肠癌指南新增了基于循环肿瘤DNA(ctDNA)的液体活检用于复发风险评估和提供预后预测信息的内容,标志基于ctDNA检测的液体活检技术运用于用药指导、微小残留病灶评估、复发监测已逐渐获得临床认可。
中国尚未审批批准上市,医院在研究性采用。
后续医疗市场的变化待观察。
3 思考为何需要下此决心
在2019年华大基因的净利润不足3.0亿元,向美国Natera,Inc.购买ctDNA技术发费2.95亿元?
目前看,同样属于一项重大决策。
获取:快速获取1/万检测限的关键技术;
拓展:将技术拓展到其他肿瘤领域,将技术适用范围拓展到常见肿瘤,而非某一种;技术适用范围拓展到用药指导、微小残留病灶评估、复发监测
快速实现:肿瘤流域的全方位技术领先。
推广:将技术示范性移植使用到华大智造的测序仪,推进华大智造的仪器覆盖肿瘤流域。(生育领域已经实现领先性国内占领)
启发:将技术运用到产品,将产品改造升级,再到市场推广覆盖是一个系统工程。
4 过去4年三件相互关联的事件
事件1:购买并改造Signatera技术
事件2:用华大因源与华大数极的股权融资5.9亿为事件2
事件3:两次股权激励行为