根据激素受体(HR)及人表皮生长因子受体2(HER2)的状态,乳腺癌可以分为三种常见的类型,即HR+/HER2-、HR-/HER2+和HR-/HER2-(三阴性乳腺癌)。HR+/HER2-是最常见的类型,占中国所有乳腺癌患者的62.0%,而HER2+约占22.4%。乳腺癌的治疗方案亦是基于HR 和HER2 的状态来进行选择。而CDK4/6 抑制剂联合其他方案是HR 阳性患者在不同阶段的最佳或一线治疗方案。PS:摘自嘉和生物招股说明书。
乳腺癌的药物研发以抗体类药物为主,其中HER2是抗体研发的主要靶点。化药小分子研发则以EGFR、HER2、CDK4&6为主要靶点。
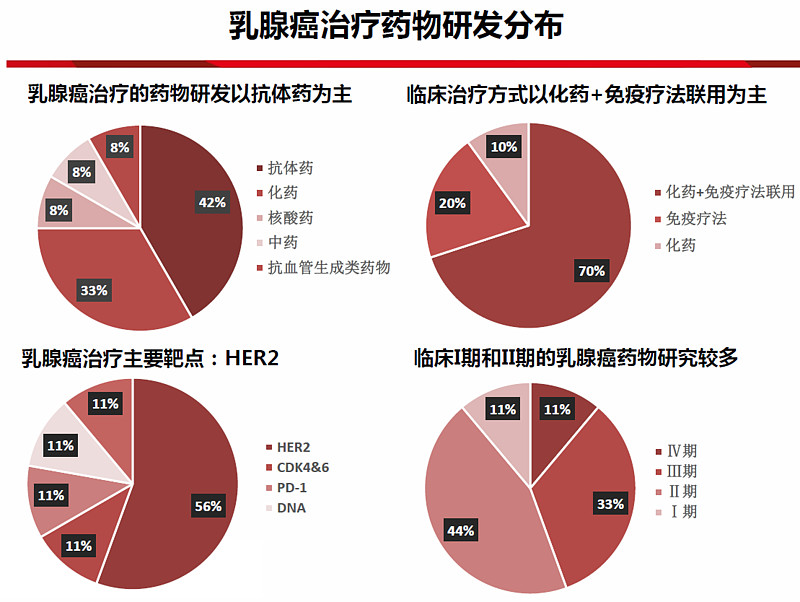
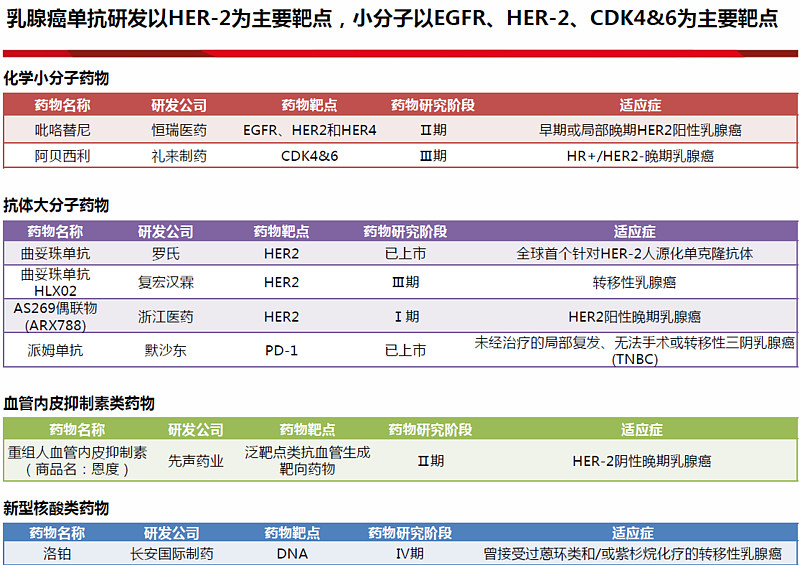
曲妥珠单抗+帕妥珠单抗+化疗联合疗法已成为HER2 阳性晚期乳腺癌的一线标准疗法,以及HER2 阳性早期乳腺癌的新辅助或辅助治疗的标准疗法。Kadcyla(T-DM1)在国内于2020 年2 月获批用于接受了紫杉烷类联合曲妥珠单抗为基础的新辅助治疗后仍残存侵袭性病灶的HER2 阳性早期乳腺癌的辅助治疗,同时CSCO 指南也将T-DM1列为曲妥珠单抗治疗失败的HER2 阳性晚期乳腺癌的二线疗法。
HR阳性/HER2阴性乳腺癌
早期乳腺癌通过激素疗法治疗,通常生命可持续5-10年。中度和高危疾病患者也可以在激素治疗之前接受化学疗法。转移性疾病的一线治疗标准是细胞周期蛋白依赖性激酶4和6(CDK4/6)抑制剂——哌柏西利/palbociclib(Ibrance,辉瑞),ribociclib(Kisqali,诺华)或阿贝西利/abemaciclib(Verzenio/Verzenios/Virginio,礼来)——联合内分泌治疗。这些疗法在2015–2017年获得了FDA的批准,并已获得标签适应症扩展;在后期试验中也对该类药物作为早期疾病的辅助治疗进行了评估。例如,评估阿贝西利关键性monarchE临床试验已达到其无浸润性疾病生存期(IDFS)主要终点。
在2019年,FDA批准了PI3K抑制剂alpelisib(Piqray,诺华)用于内分泌治疗进展后发生PIK3CA突变(约40%患者)的晚期或转移性疾病。依维莫司/everolimus(Afinitor,诺华)联合依西美坦也是HR阳性/HER2阴性复发性疾病的治疗选择。
一、HER2阳性乳腺癌:
1)恩美曲妥珠单抗,Kadcyla,T-DM1:在乳腺癌中最为著名的耦联体药物,结合了化疗和曲妥珠单抗的优点,主要针对HER2阳性的乳腺癌。网页链接
2)DS-8201,Trastuzumab Deruxtecan,Enhertu:对HER2阳性乳腺癌发挥出令人满意的疗效;网页链接;
二、三阴性乳腺癌(TNBC)
1)Trodelvy(ADC)(已美国获批上市)
临床试验ASCENT,共纳入108名患者,总缓解率(ORR)达33.3%,中位缓解持续时间(mDoR)为7.7个月。持续缓解的患者中:55.6%的患者缓解持续时间超过6个月,16.7%的患者缓解持续时间超过12个月。因在三线治疗三阴乳腺癌中疗效突出,经独立数据监督委员会审评,提前停止了3期临床试验。
FDA批准是基于一项多中心、单臂、II期临床试验(IMMU-132-01)中的ORR和DOR数据。在 108例入组患者中,接受Trodelvy治疗的患者组客观缓解率高达33.3%,其中包含2.8%的完全缓解率和30.6%的部分缓解率。远高于传统的化疗组疗效。
疾病控制率高达74.1%,其中37%的患者疾病稳定。到数据截至时,有6例患者临床疗效持续了12个月以上,最长的达到了30.7个月。中位PFS是5.5个月,中位OS为13个月。
安全性方面,最常见的不良事件是恶心(67%)、中性粒细胞减少(64%)、腹泻(62%)、疲劳(55%)和贫血(50%)。网页链接
Trodelvy的活性药物成分为sacituzumab govitecan,这是一种新型、首创的抗体药物偶联物(ADC),由靶向TROP-2抗原的人源化IgG1抗体与化疗药物伊立替康(一种拓扑异构酶I抑制剂)的代谢活性产物SN-38偶联而成。TROP-2是一种在90%以上的TNBC中表达的细胞表面糖蛋白。 $吉利德科学(GILD)$ $云顶新耀-B(01952)$
2)KN046(PD-L1/CTLA-4)网页链接
KN046-203(NCT03872791)是一项Ⅰb/Ⅱ期、开放、多中心的临床研究,旨在评估KN046联合白蛋白结合型紫杉醇在晚期三阴乳腺癌受试者中的有效性、安全性和耐受性。研究共入组27例初治局部晚期不可切除或转移性三阴乳腺癌女性患者。结果显示KN046耐受性良好,KN046联合白蛋白结合型紫杉醇对晚期三阴乳腺癌患者有效,特别是在PD-L1阳性的三阴乳腺癌患者中显示出了潜在的无进展生存期(PFS)和初步总生存期(OS)获益:
截至2021年3月8日,25例可评估的三阴乳腺癌患者的客观缓解率(ORR)为40.0%,疾病控制率(DCR)为96.0%。中位随访时间13.7个月。意向性人群的中位无进展生存期(PFS)为7.3个月(95%CI: 3.7~NE)。中位总生存期(mOS)未达到,意向性人群的15个月OS率为73.4% (95% CI:46.1~88.4%)。在PD-L1阳性 (IC PD-L1≥1%) 患者中,中位PFS为13.8个月 (95% CI:1.6~NE),15个月的OS率为77.1% (95% CI:34.5~93.9%)。
截至2021年3月8日,无KN046治疗相关的死亡案例发生;13例患者(48.1%)发生3-4级KN046治疗相关的不良事件(AE);4例患者(14.8%)发生KN046治疗相关的严重不良事件(SAE);11例患者(40.7%)发生免疫相关不良事件(irAEs);大部分irAEs为1-2级,仅有3例患者发生3级irAEs,分别为2例3级免疫介导性肝病和1例3级皮疹。 网页链接{$康宁杰瑞制药-B(09966)$}
3)K药(已上市PD-1)网页链接
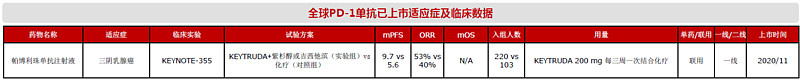
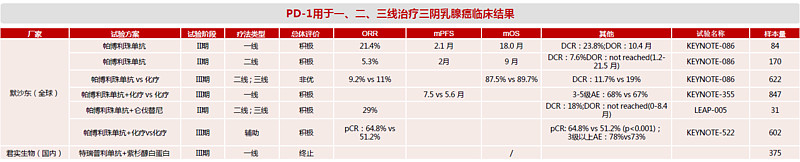
KEYNOTE-355(注册号:NCT02819518)是一项随机、双盲、安慰剂对照的Ⅲ期临床试验,在29个国家的209个中心开展。在2017年1月9日至2018年6月12日期间,研究共入组847例未经治疗的局部复发不能手术或转移性TNBC患者,按2:1随机分为两组。其中,实验组566例患者接受每3周1次的200mg帕博利珠单抗联合化疗(白蛋白紫杉醇,紫杉醇或吉西他滨联合卡铂),对照组281例患者接受每3周1次安慰剂联合化疗。KEYNOTE-355研究的主要疗效评估终点是两组PD-L1 CPS≥10、CPS≥1以及意向治疗人群的无进展生存期(progression-free survival,PFS)和总生存期(overall survival,OS)。研究已在中期分析中对相关人群PFS进行了明确评估;目前仍在继续进行随访,以评估总体生存率。
研究结果
在第二次中期分析时,帕博利珠单抗联合化疗组的中位随访时间为25.9(IQR 22.8~29.9)个月,安慰剂联合化疗组的中位随访时间为26.3(IQR 22.7~29.7)个月。
分层分析显示,随着PD-L1表达水平的上升,化疗联用帕博利珠单抗的方案治疗效果增强。在PD-L1 CPS≥10的TNBC患者群体中,帕博利珠单抗联合化疗组的中位PFS为9.7个月,明显长于安慰剂联合化疗组的5.6个月(HR = 0.65,95% CI 0.49-0.86;P = 0.0012)(图1;表1)至于安全性方面,3~5级治疗相关不良事件发生率在帕博利珠单抗联合化疗组为68%,在安慰剂联合化疗组为67%;其中,帕博利珠单抗联合化疗组死亡率<1%,安慰剂化疗组为0%。两组治疗方案导致不良事件的情况无显著差异,证实联合方案的耐受性与传统化疗基本一致,添加帕博利珠单抗并未给传统化疗方案带来更多安全问题。
4)阿替利珠单抗(PD-L1)网页链接
III期的IMpassion130试验中,阿替利珠单抗(泰圣奇)联合白蛋白紫杉醇与安慰剂联合白蛋白紫杉醇进行效果对比。阿替利珠单抗联合白蛋白紫杉醇的方案在PD-L1阳性的三阴乳腺癌患者中,可使疾病进展或死亡风险显著降低40%(中位PFS:7.4个月 vs 4.8个月,HR=0.60,95%CI:0.48-0.77,p<0.0001)、使总生存期(OS)表现出7个月的临床意义改善(中位OS:25.0 vs 18.0个月,HR=0.71,95%CI:0.54-0.93)。
PS:癌症2020数据统计:
1)2020年全球发病率前十的癌症分别是:乳腺癌226 万, 肺癌220 万,结直肠癌193 万,前列腺癌 141 万,胃癌 109 万,肝癌 91 万,宫颈癌60 万,食管癌 60 万,甲状腺癌 59 万,膀胱癌57 万,这十种癌症占据新发癌症总数的 63%。癌症死亡人数前十的癌症分别是:肺癌180 万,结直肠癌94 万, 肝癌83 万,胃癌 77 万,乳腺癌68 万,食管癌54 万,胰腺癌 47 万,前列腺癌38 万,宫颈癌34 万,白血病31 万,这十种癌症占据癌症死亡总数的 71%。
1a)2020 年全球男性新发癌症 1007 万例,占总数的 52%, 全球男性新发病例数前十的癌症分别是: 肺癌144 万,前列腺癌141 万,结直肠癌 107 万,胃癌 72 万,肝癌63 万,膀胱癌44 万,食管癌42 万,非霍奇金淋巴瘤30 万, 肾癌27 万,白血病27 万,这十种癌症占男性新发癌症总数的近 70%。2020 年全球男性癌症死亡 553 万例,占总数的 56%,其中肺癌死亡人数达 119 万人,远超其他癌症类型,2020 年 全球男性癌症死亡人数前十的癌症分别是: 肺癌 119 万,肝癌58 万,结直肠癌52 万,胃癌50 万,前列腺癌 38 万,食管癌37 万,胰腺癌 37 万,白血病18 万,膀胱癌16 万, 非霍奇金淋巴瘤15 万,这十种癌症占男性癌症死亡总数的近 77%。
1b)2020 年全球女性新发癌症 923 万例,占总数的 48%,2020 年女性乳腺癌新发 226 万例,远超女性其他癌症类型。全球女性新发病例数前十的癌症分别是:乳腺癌226 万,结直肠癌87 万,肺癌77 万,宫颈癌60 万,甲状腺癌 45 万,子宫内膜癌42 万,胃癌37 万,卵巢癌31 万,肝癌27 万,非霍奇金淋巴瘤24 万,这十种癌症占女性新发癌症数的 71%。2020 年全球女性癌症死亡 443 万例,占总数的 44%,2020 年全球女性癌症死亡人数前十的癌症分别是:乳腺癌68 万,肺癌61 万, 结直肠癌42 万,宫颈癌 34 万,胃癌27 万,肝癌25 万,胰腺癌 22 万,卵巢癌21 万,食管癌 17 万,白血病13 万,这十种癌症占女性癌症死亡总数的近 74%。
2)2020 年中国癌症新发病例数前十的癌症分别是:肺癌82 万,结直肠癌56 万,胃癌48 万,乳腺癌42 万,肝癌41 万,食管癌32 万,甲状腺癌 22 万,胰腺癌 12 万,前列腺癌 12 万,宫颈癌 11 万,这十种癌症占新发癌症数的 78%。2020 年中国癌症死亡人数前十的癌症分别是:肺癌71 万,肝癌39 万,胃癌 37 万,食管癌30 万,结直肠癌29 万,胰腺癌12 万,乳腺癌12 万,神经系统癌症7 万,白血病6 万,宫颈癌6 万,这十种癌症占癌症死亡总数的 83%。
2a)2020 年中国男性癌症新发病例数248万;前十的癌症分别是:肺癌54 万,胃癌33 万,结直肠癌32 万,肝癌30 万,食管癌22 万,前列腺癌12 万,胰腺癌7 万,膀胱癌 7 万,甲状腺癌 5 万,非霍奇金淋巴瘤 5 万,这十种癌症占男性新发癌症数 84%。2020 年中国男性癌症死亡病例数 182 万,占总数的 61%,其中肺癌、肝癌、胃癌、食管癌死亡数最多。
2b)2020 年中国女性癌症新发病例数209万;前十的癌症分别是:乳腺癌42 万,肺癌28 万,结直肠癌24 万,甲状腺癌17 万,胃癌15 万,宫颈癌11 万,肝癌 11 万,食管癌 10 万,子宫内膜癌 8 万,卵巢癌6 万,这十种癌症占女性新发癌症数 81%。2020 年中国女性癌症死亡病例数118万;前十的癌症分别是:肺癌24 万,结直肠癌 12 万,胃癌12 万,乳腺癌12 万,肝癌10 万,食管癌 9 万,宫颈癌6 万,胰腺癌 5 万,卵巢癌4 万,神经系统癌症 3 万,这十种癌症占癌症死亡总数的 83%。