快 讯
2024-1-24,致力于开发治疗代谢性疾病创新疗法的先为达生物宣布了其在研口服多肽减肥药伊诺格鲁肽(XW004,Oral Ecnoglutide)片剂Ⅰ期临床试验已完成的4个试验组取得积极结果。
该项Ⅰ期临床试验(NCT05184322)是一项随机、双盲、安慰剂对照的多次剂量递增研究,在澳大利亚共招募42名健康受试者(第1-3试验组)和14名健康肥胖受试者(第4试验组)。受试者随机接受每日一次口服伊诺格鲁肽或安慰剂口服片剂。
第1-3试验组的受试者平均基线体重为75.6至77.9公斤,平均BMI为25.8至26.1 kg/m²;第4试验组的受试者平均基线体重为100.1公斤,平均BMI为32.9kg/m²。口服伊诺格鲁肽的目标剂量在第1-3试验组分别为7 mg、15 mg或30 mg,为期2周;在第4试验组的目标剂量为30 mg,为期6周,其中包含剂量递增期。该研究主要评估项目包括口服伊诺格鲁肽的安全性、耐受性、药代动力学和受试者平均体重相对基线的变化。
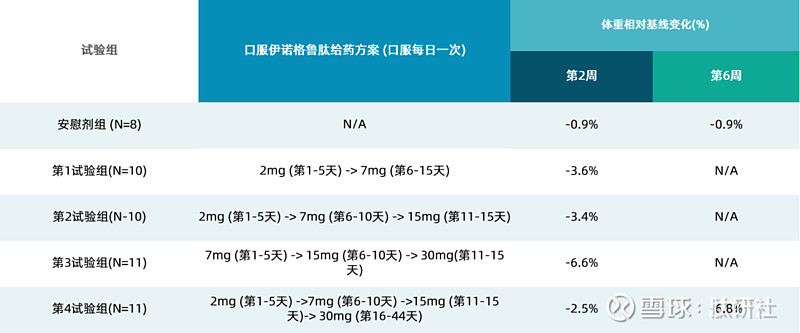
图1. XW004临床数据
刚出炉的Ⅰ期临床数据显示,在第1-3试验组的治疗2周后体重相对基线变化分别为-3.6%、-3.4%和-6.6%,而安慰剂组为-0.9%,即相对安慰剂组减重分别为2.7%、2.5%、5.7%;第4试验组治疗6周后体重相对基线变化-6.8%,安慰剂调整后减重5.9%。
安全性方面,口服伊诺格鲁肽的总体安全性和耐受性与肽类GLP-1激动剂的已知安全性特征一致,最常见的不良事件包括恶心、头痛、腹泻、呕吐和食欲减退,大多数不良事件的严重程度为轻中度,主要发生在剂量递增期。
先为达生物表示,基于以上4个试验组的积极结果,该项临床研究在继续进行中、旨在进一步评估包括肥胖受试者每周一次口服给药的治疗方案。
口服技术得以验证
与司美格鲁肽相似,对于伊诺格鲁肽,先为达生物同时推进注射剂型与口服型的临床研究,注射版本代号为XW003,口服版本代号为XW004。
其中,注射版本XW003用于治疗肥胖症和2型糖尿病的临床目前已进入Ⅲ期,CKD和NASH进入Ⅰ期。伊诺格鲁肽在临床中显示出较好的降糖和减重的水平,这也是先为达推进口服剂型的底气。
一项在澳大利亚和新西兰成年肥胖症患者中开展的减重疗效临床数据显示,治疗26周后,伊诺格鲁肽1.2mg、1.8mg和2.4mg组的受试者体重分别较基线降低11.5%、11.2%和14.7%(2.4mg组,P<0.001)。一项评估伊诺格鲁肽在中国2型糖尿病患者中的疗效数据显示,在治疗20周时,伊诺格鲁肽组的受试者糖化血红蛋白(HbA1c)较基线显著降低1.81% 至2.39%,安慰剂组则降低0.55%(P<0.0001)。
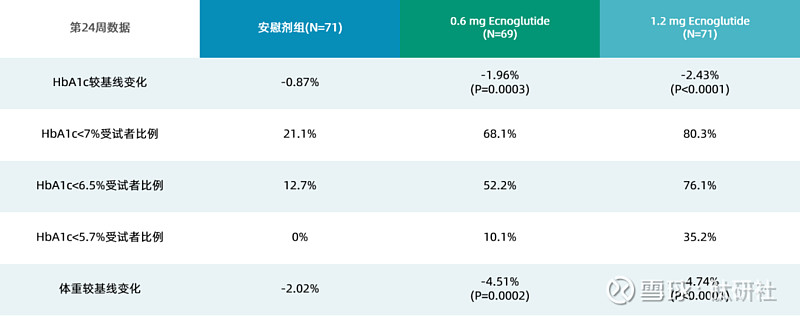
图2. XW004降糖临床数据
本次发布临床积极数据的XW004是伊诺格鲁肽的每日一次的口服剂型。先为达在口服技术上应用了渗透增强剂的策略,该策略也是临床上运用最广泛的改善多肽口服吸收的递送策略之一,可以通过促进多肽采取跨细胞途径通过上皮细胞,或者利用细胞旁途径,干扰细胞间连接蛋白和粘附蛋白而进入系统循环。
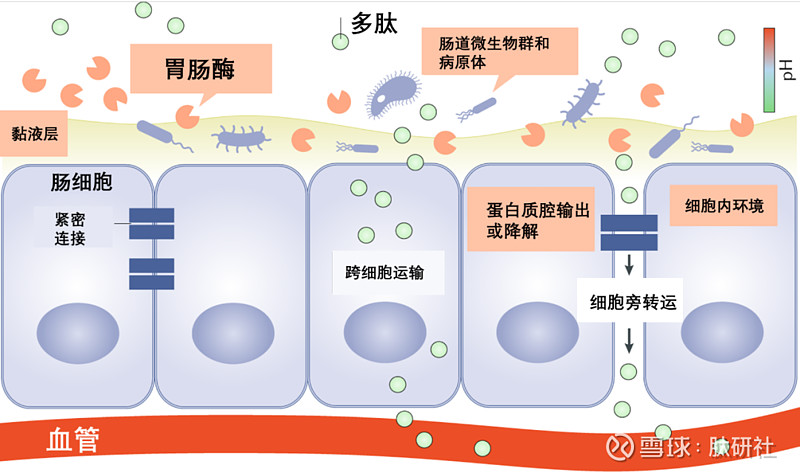
图3. 肠道结构示意图以及对口服多肽吸收的挑战
目前,临床上应用的最成熟的两种渗透促进剂分别是癸酸钠(C10,也称为癸酸)和N-[8-(2-羟基苯甲酰基)氨基]辛酸钠(SNAC,也被称为沙卡普罗酸钠),已经在专利的输送平台上使用了很多年,并且已经在人体内进行了比其他任何增强剂更广泛的试验。
先为达在专利布局上基于以上两种渗透剂进行改进和组合,并加入铋剂以增加生物利用度并降低用量。
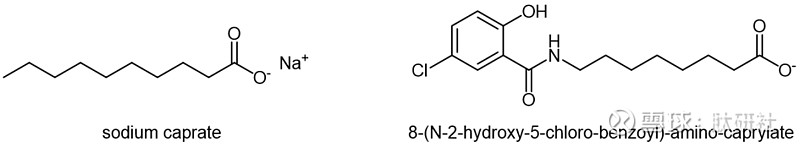
图4. 癸酸钠/辛酸钠示意图
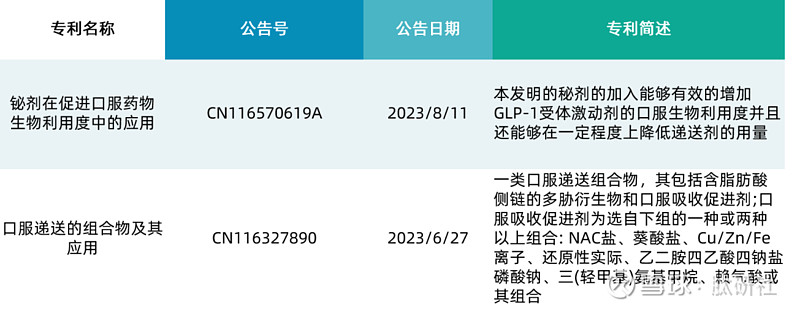
具体而言,根据先为达在口服多肽领域布局了两个专利:一个是口服递送组合物专利(专利号:CN116327890A),所述口服吸收促进剂为选自下组的一种或两种以上的组合:NAC盐、癸酸盐、Cu、Zn、Fe离子、还原性试剂、乙二胺四乙酸四钠盐、磷酸钠、三(羟甲基)氨基甲烷、赖氨酸、或其组合;另一个是铋剂的应用(专利号:CN116570619A)。
表1.先为达口服多肽专利信息
本次临床数据的公布初步说明了先为达口服多肽技术的成功应用,初步临床结果显示,口服多肽的生物利用度较司美格鲁肽约有3-5倍提升。
从临床减重疗效来看,30 mg组6周平均减重6.8%的成绩,都优于LIlly的口服小分子Orforglipron 24/45mg剂量组和硕迪生物的小分子GSBR-1290 120mg剂量组在第6周的数据。与口服司美格鲁肽相比,在PIONEER PLUS临床中,入组患者基线体重96.4kg,口服司美格鲁肽25mg剂量组在68周的时间减重7kg,接近减重7.3%,XW004在6周的时间就已接近口服司美格鲁肽68周的数据,数据较积极。
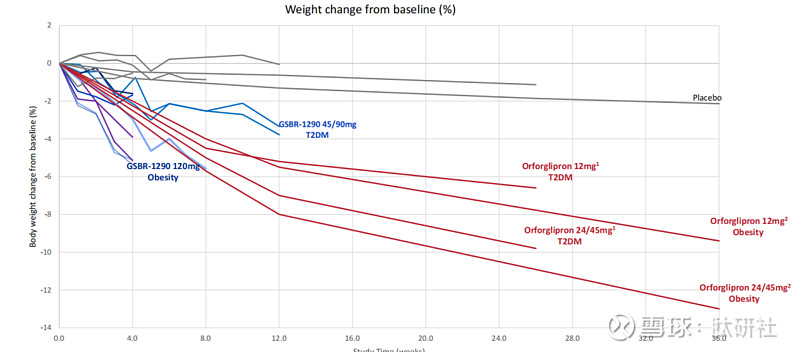
图5. Orforglipron 与GSBR-1290临床数据
接下来,先为达生物需要开展入组人数更多、临床时间更长的的Ⅱ期临床,以验证口服多肽XW004的是否具有持续减重的趋势。
关于先为达生物
先为达生物成立于2017年,是一家聚焦代谢性疾病领域生物大分子新药开发生物医药企业,总部位于杭州,研发和国内注册中心位于北京,并先后在澳大利亚、美国设立全资子公司,分别负责海外临床开发,海外注册申报和BD业务,另外在上海也设有办公室。
截至目前,先为达已累积完成6轮融资,融资金额超过10亿元,获得IDG资本、正心谷资本、LYFE Capital、君联资本、拾玉资本、海邦投资等机构的支持。
管理团队方面,有经验的团队是临床管线得以快速推进的基础,先为达管理团队既有来自Amgen、Lilly、Gilead、Novartis、Novo Nordisk和GSK等跨国企业的自身科学家,也有来自本土创新药研发企业的人才。创始人是潘海博士,美国内布拉斯加州立大学生物化学博士,拥有超过25年生物医药从业经历,先后就职于Amgen、凯因科技等领先生物医药企业。
研发管线方面,先为达生物专注于代谢疾病疗法的开发,围绕GLP-1靶点,除了开发了多肽类型降糖减肥药XW003和XW004,还开发了小分子XW014,目前已在美国开展Ⅰ期临床,数据未披露。此外,还开发了双靶点组合疗法XW017+XW003,其中XW017是一种新型、长效的GIP肽类似物,针对生物活性和体内稳定性进行了优化,为肥胖症、2型糖尿病和NASH提供更有效的联合疗法。
除了代谢疾病领域,针对感染疾病领域,先为达还开发了XW001干扰素λ吸入溶液,其在人源干扰素λ 1的基础上,经蛋白质工程优化,使得雾化吸入给药更加稳定。XW001具有独特的广谱抗病毒优势,临床前研究显示,其可显著降低呼吸道合胞病毒、流感病毒、偏肺病毒等的复制。此外,XW001可显著抑制新冠病毒的复制,并可明显降低感染造成的肺部炎症。
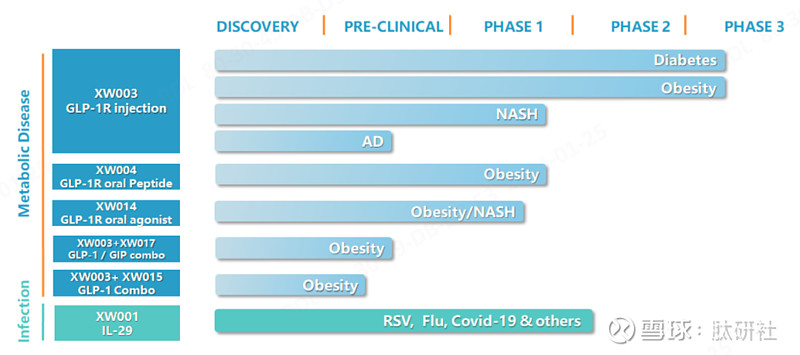
图6. 先为达生物临床管线
| 引用资料
[1] 肽研社:上下而求索-口服多肽发展之路
[2] 猎药人俱乐部:卧虎藏龙!国内GLP-1布局企业大有看头
[3] 先为达生物:先为达宣布口服伊诺格鲁肽(XW004,Oral Ecnoglutide)Ⅰ期临床试验取得积极结果
[4]先为达官网