去年3期最后一例是11月入组,因此后续动态提交数据,最晚年底申报了。其次,竞争格局变化不大,后续开三期的,不管是JAK还是IL4R,都需要做52周才能申报。
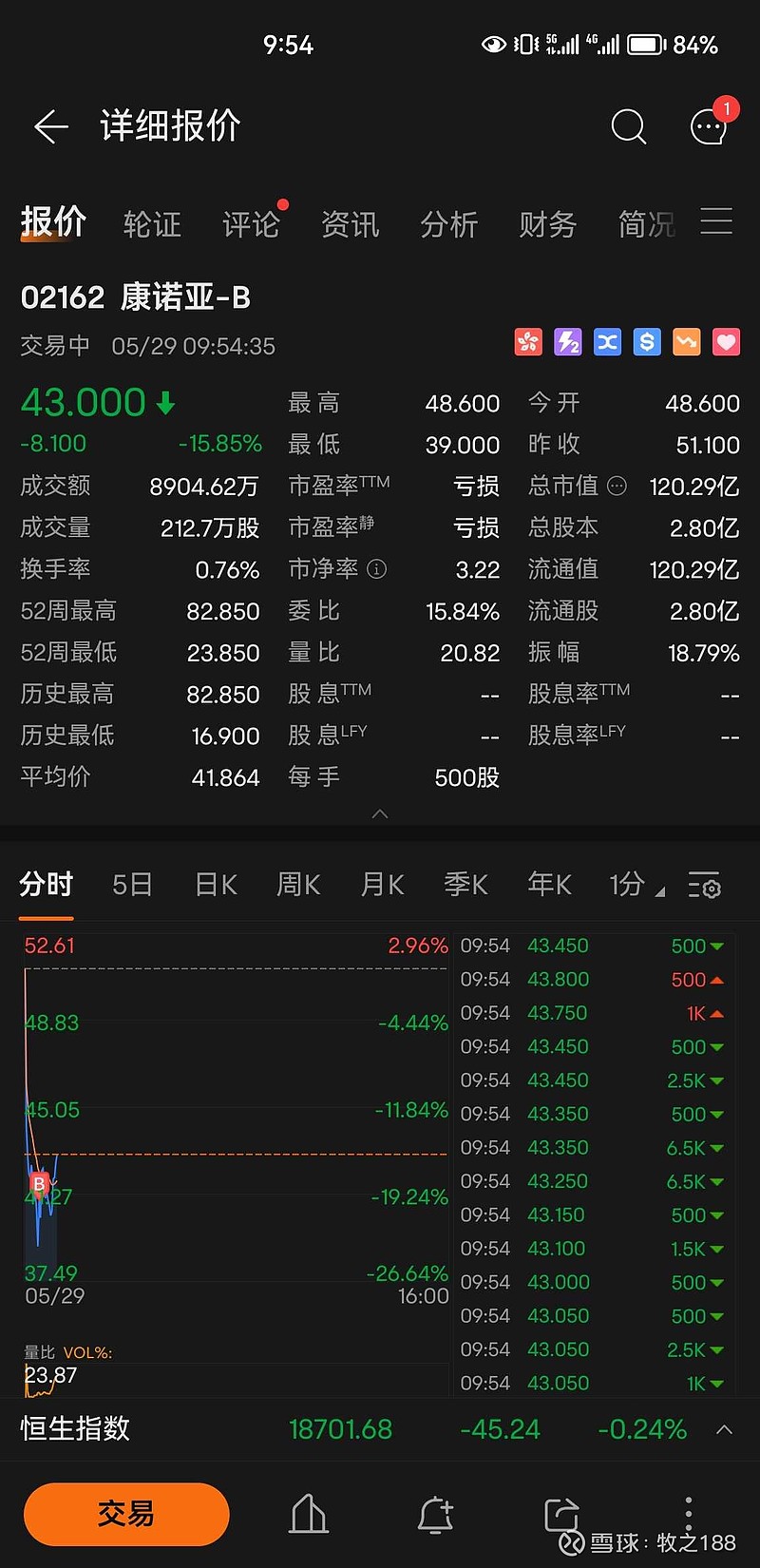
就这点事,利空影响肯定是有的,但不至于这样,跌下来是机会,毕竟不是成药的问题,39.8加了点。能跌下来,继续网格加吧。
| 发布于: | Android | 转发:6 | 回复:26 | 喜欢:1 |

跌下来就是机会
主要是原本也涨了太多,现在市场一点风吹草低就崩盘
康诺亚这个是需要补充患者还是原有患者直接随访到52周就可以?如果新增患者,要一年多。$康诺亚-B(02162)$
其实一般有经验的团队,应该在一开始的时候就入组52周组的患者先,然后36周,然后再12周,这样数据基本可以同时成熟。
慢病领域,很对产品都要求一年数据,这个在开III期的时候,CDE沟通为啥不提出要求呢?有点不明白。
老师,推后上市,是否会影响到后面进入医保的节奏?
“310延期3个月到6个月申报”,这个是哪里看到的消息?[好困惑]
同一适应症,怎么可能有差别?jak1也得走这个周期。
下跌是有点凶,有点美股的味道。之前公司给的预期有点乐观,52周申报应该不是啥新鲜事,临床开发的人应该有所预期。大概率国产JAK1领先于康诺亚拿到AD适应症,后面看销售?IL-4α比JAK1安全性更好是事实,但在国内市场份额如何分布?有人有dupi和现在两个进口JAK1(upa 和 abro )在AD的销售数据吗?
近20年,刚股和爱股市场都是全球最差投资市场