文章来源:“凯莱英药闻”微信公众号
4月19日,纳斯达克上市公司Anixa Biosciences宣布其与莫菲特癌症中心(MCC)共同开发的卵巢癌CAR-T疗法临床试验申请(IND)遭FDA搁置,需补充申请资料以获FDA授权开展临床试验,FDA将在30日给予更详细的答复函。

受此消息影响,Anixa Biosciences股价当日最高跌幅达18.9%,收盘价4.06美元,跌幅13.6%。
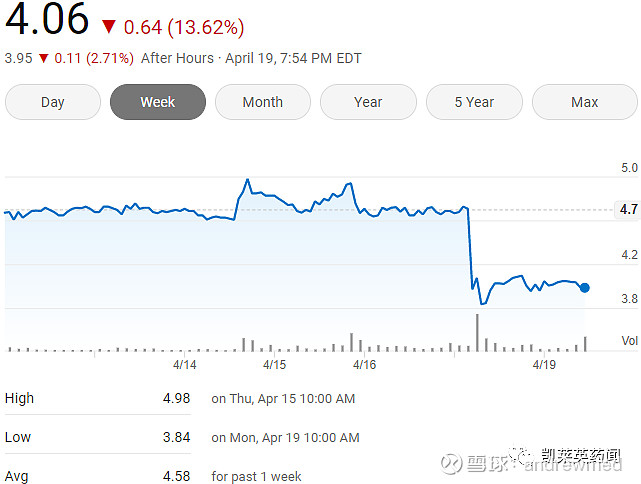
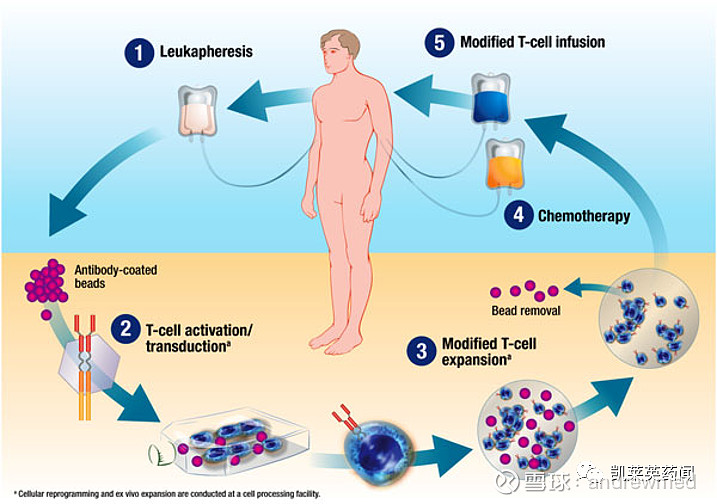
该卵巢癌CAR-T疗法采用自体细胞扩增技术,为每一位患者单独制造成品药(由靶向卵巢免疫特有的促卵泡激素受体(FSHR)工程化T细胞组成)。
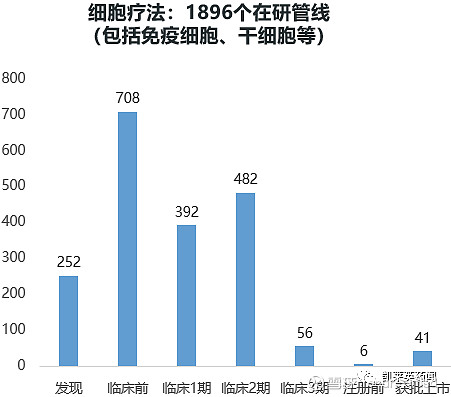
当前,包括干细胞、免疫细胞在内的细胞疗法全球范围内已有1896个在研管线。自FDA于2017年批准全球首款CAR-T疗法上市,目前上市CAR-T产品达到5款,其中靶向CD19的有4款产品,1款靶向BCMA,获批适应症包括:原发纵隔B细胞淋巴瘤、多发性骨髓瘤、套细胞淋巴瘤、弥漫性大B细胞淋巴瘤、急性淋巴细胞白血病和滤泡性淋巴瘤等。
单一靶点CAR-T疗法易因抗原丢失或下调导致病情复发,威斯康星医学院研究人员设计出靶向CD19和CD20的新型CAR-T疗法,并于nature子刊nature medicine公布I期临床数据,接受最高剂量(fresh infusion)2.5 x10^6 CAR-20/19-T的12位患者应答率达到100%,全部剂量下患者应答率为82%。

贝勒医学院的研究人员更是开发出同时靶向CD19、CD20 及CD22的三特异性duoCAR-T疗法,并在体外及小鼠试验模型中验证该疗法的抗肿瘤活性。
新靶点和新技术为细胞疗法不断打开成功之门,然而当前细胞疗法生产技术的成熟程度远低于化药、单抗等,开发细胞疗法的企业进行创新疗法开发的同时,把好质量关、做好注册申报、降低审批时间成本也同样重要。
版权说明:本文来自凯莱英,感谢关注、转发。欢迎媒体/机构转载,转载请注明来自“凯莱英药闻”。