2024年3月20日,中国沈阳
今天,中国生物制药领军企业三生制药(01530.HK)公布年度业绩。
业绩公告显示,2023年三生制药营业收入约人民币78.16亿元,比去年同期增长13.8%;毛利约人民币66.42亿元,比去年同期增长17.1%;经调整的经营性归母净利润约人民币19.52亿元,比去年同期增长17.7%;经调整EBITDA约人民币27.68亿元,比去年同期增长20.2%。
同时,三生制药董事会建议宣派截至2023年12月31日止年度的末期股息每股0.25港币。
核心产品业绩稳健,生物药板块持续增长
2023年,三生制药核心生物药产品营收保持强劲增长,稳居行业龙头。全球唯一商业化的重组人血小板生成素(rhTPO)产品特比澳销售收入约42.05亿元,同比增长23.8%。该产品已顺利续约医保,并被《中国临床肿瘤学会(CSCO)肿瘤治疗所致血小板减少症诊疗(CTIT)指南(2022版)》列为最高级别推荐。
促红素双品牌益比奥和赛博尔2023年销售收入为9.4亿元,根据艾昆纬(IQVIA)数据其市场份额达42.2%。
用于治疗类风湿性关节炎、强直性脊柱炎及银屑病的益赛普2023年销售收入5.65亿元,同比增长10.5%。益赛普预充针剂型于2023年3月获批上市。
用于治疗HER2阳性转移性乳腺癌的赛普汀2023年销售收入为2.26亿元,同比大幅增加41.8%。该产品获得中国临床肿瘤学会《乳腺癌诊疗指南(2022)》HER2阳性晚期乳腺癌H治疗敏感用药I级推荐,同时开展了大量真实世界研究和临床专家发起的研究,循证证据不断丰富。
毛发健康产品持续丰富,蔓迪市占率达72.6%
治疗雄激素性脱发和斑秃的OTC产品蔓迪继续保持快速增长趋势。2023年蔓迪销售收入11.24亿元,同比增加约25.8%。中国药学会数据显示,蔓迪在中国大陆米诺地尔市场的占有率达72.6%。2023年,蔓迪持续打造科学生发品牌,拓展数字化营销体系,提升电商销售规模。此外,蔓迪泡沫剂型产品成功获批上市,将进一步助力蔓迪未来在市场竞争格局中占据优势地位。
CDMO业务再创新高
2023年,三生制药CDMO业务规模持续提升,收入约人民币1.74亿元,同比增长4.9%。目前公司已签订的订单金额约人民币2亿元,客户覆盖国内外知名药企和生物科技公司。沈阳德生生物7.6万升原液及制剂产能已于2023年起陆续开始验证。
在研管线开发全面驶入快车道
公告显示,三生制药研发管线拥有29项在研产品,包含血液/肿瘤科13项,自身免疫及眼科11项,肾科4项,皮肤科领域1项。截至目前,已有12款新药推进至临床III期或NDA申报阶段,3款仿制药品种处于BE及ANDA申报的阶段。
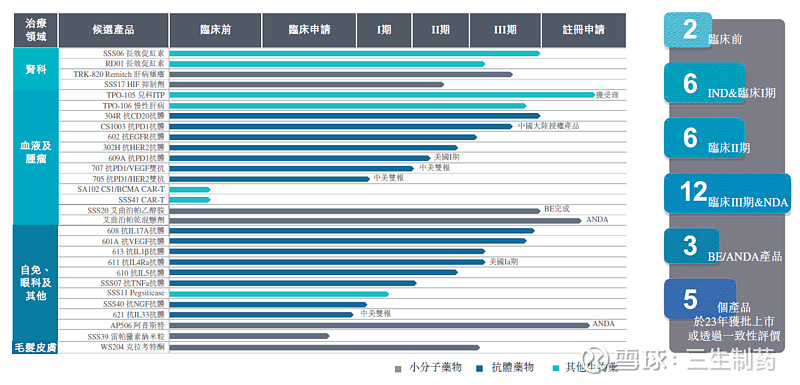
2023年,三生制药多款产品获批上市,其中包括:益赛普预充针剂型,其为患者提供了更加便利的治疗选择,显著提高使用环节的便利性;盐酸纳呋拉啡口腔崩解片丽美治®用于血液透析患者瘙痒的适应症,同时该产品用于改善慢性肝病患者瘙痒症(仅限现有治疗疗效不理想的情况)的III期临床试验申请已获批准,预计将在本年度提交NDA申请。此外,米诺地尔泡沫剂型已于2023年12月获批上市,满足头皮敏感人群的生发用药需求。长效促红素(SSS06)用于慢性肾衰竭贫血治疗的III期临床研究达到主要预设终点,公司计划于今年内递交该产品新药上市申请。
自免管线即将迎来收获期。2023年,用于治疗斑块状银屑病的抗IL-17A抗体(608)治疗斑块状银屑病的III期临床试验已达到主要终点,预计将于今年完成该适应症的BLA(生物制品许可申请)申报;用于治疗急性痛风性关节炎的抗IL-1β抗体(613)和治疗特应性皮炎、慢性鼻窦炎伴鼻息肉和中重度慢性阻塞性肺气肿的IL-4Rα抗体(611)II期临床成功达到主要终点,并已完成III期临床试验患者入组;用于治疗哮喘的抗IL-5抗体(610)已获得重度嗜酸性粒细胞哮喘的II期临床研究的主要终点数据。
2023年,三生制药对外合作取得多项进展。三生制药与基石药业合作开发的抗PD-1单抗Nofazinlimab的III期临床研究正在积极推进中。依托三生制药丰富的抗体药研发注册经验,高质量、高性价比的生产能力和成熟的肿瘤商业化团队,该产品有望为晚期肝细胞癌患者带来全新优效的一线治疗选择。公司与Cosmo合作的克拉考特酮乳膏Winlevi®用于痤疮适应症的桥接临床试验已获国家药监局批准.作为FDA 40年来批准的首个新机制痤疮用药,Winlevi®在美国获得皮肤科医生的广泛认可,自2021年12月上市以来有1.5万名医生开具超过67万张处方,已成为美国处方量最多的痤疮治疗用药之一。Winlevi®有望在三生制药的推动下为国内数以亿计的痤疮患者带来新的治疗选择。
未来,三生制药将继续聚焦肾科、自免、毛发皮肤、血液、肿瘤等优势领域,加速推进在中国大陆处于领先地位的自免类产品的临床开发。同时公司将持续践行自主研发和对外合作双轨并行的策略,积极发掘有潜力的创新药合作标的,以补充公司现有的产品布局。公司还将凭借成熟的生物药研发注册、商业化生产以及销售实力,为更多优质创新药产品的研发上市进程提供助力。
三生制药董事长兼首席执行官娄竞博士表示:“在过去的一年里,面对机遇与挑战并存的行业环境,三生制药全体员工同德一心,共同推进各项业务平稳发展,业绩再创新高。我们非常欣喜地看到公司不断向市场推出新产品,让患者享受到全新的治疗获益,并且期待后续管线中的在研产品逐步展露潜力,为公司发展持续打造新增长引擎。同时,三生制药还将充分发挥综合平台优势,为海内外生物技术企业赋能。未来,三生制药将继续牢记民族生物制药企业的责任,在制药为人的道路上沉淀阅历、汇聚能量,厚植企业成长之本,夯实产业进步之基,为促进行业高质量发展添砖加瓦,为助力健康中国建设贡献力量。”
关于三生制药
三生制药是一家集研发、生产和销售为一体的生物制药领军企业,致力于以高品质的药品提高患者生存质量,为人类健康造福。目前,公司拥有100余项国家发明专利授权,40余种上市产品,覆盖肾科、肿瘤科、自身免疫性疾病、眼科及皮肤科等多种治疗领域。公司拥有抗体药物国家工程研究中心以及生物药和化药双平台的4大研发中心,共有29种在研产品,其中25种为国家新药,并拥有符合GMP标准的5大生产基地。未来,三生制药将继续秉持“珍爱生命、关注生存、创造生活”的理念,全力打造全球领先的中国生物制药企业。请访问网页链接获取更多信息。
警示说明及前瞻性陈述
本新闻稿包含前瞻性陈述,例如涉及业务和产品前景,或公司的意图、计划、认知、预期及策略。该等前瞻性陈述是根据本公司现有的资料,并按本新闻稿发布时的展望陈述。该等前瞻性陈述基于若干预测、假设及前提,其中一些是主观性的或不受我们控制。该等前瞻性陈述可能被证明是不正确的,或将来可能无法实现。就任何新产品或产品的新适应症, 我们无法确保其将能成功开发或最终上市销售。该等前瞻性陈述受各种风险及不明朗因素影响。我们的其他公开披露文件可能提供该等风险及不明朗因素的更多信息。所涉及之科学信息可能只是初步的和研究性的。本公司股东及潜在投资者在买卖本公司股份时,请务必谨慎行事。