声明:因水平有限,错误不可避免,或有些信息非最及时,欢迎留言指出。本文仅作医疗健康相关药物介绍,非治疗方案推荐(若涉及);本文不构成任何投资建议。

引言
2022年6月17日,药审中心承办了默克公司的1类化药M1774胶囊的临床申请,这是一种ATR(共济失调毛细血管扩张症和rad3相关蛋白)抑制剂。
(图源:CDE官网)
ATR
ATR是丝氨酸/苏氨酸蛋白激酶的磷脂酰肌醇3-激酶相关激酶(PIKK)家族的成员。ATR的N-末端包含ATRIP (ATR相互作用蛋白)的结合位点,调节ATR在复制应激和DNA损伤位点的定位。
ATR和ATM是DNA损伤反应(DDR)信号网络中的两种重要蛋白,它们被DNA损伤激活。ATR抑制剂通过阻断ATR介导的信号通路,可以扰乱DNA损伤修复。研究显示,在ATM缺失的肿瘤细胞中,ATR抑制剂可以产生合成致死效应,在导致ATM缺失肿瘤细胞死亡的同时,并不影响正常细胞。
合成致死
合成致死是指当两个非致死性突变基因单独发生时不会导致细胞死亡,而同时发生时可引起细胞死亡的现象。
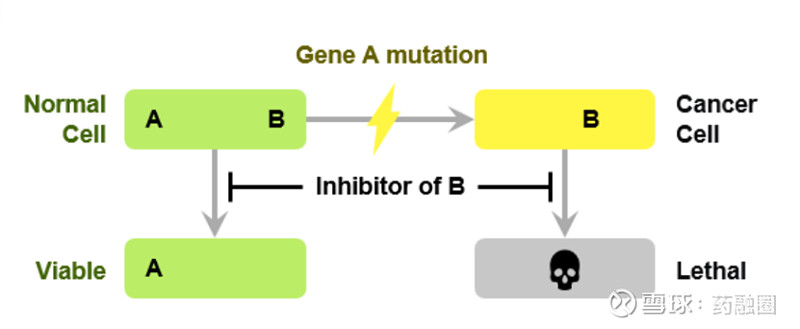
图源网页链接
目前研究最多的是基于DDR(DNA损伤反应)的合成致死机理,常用的有PARP,ATR,ATR,CHK1,CHK2,DNA-PK和Wee1,这几个靶点的共同合成致死基因是TP53,其在DNA损伤反应中的作用通路如下。
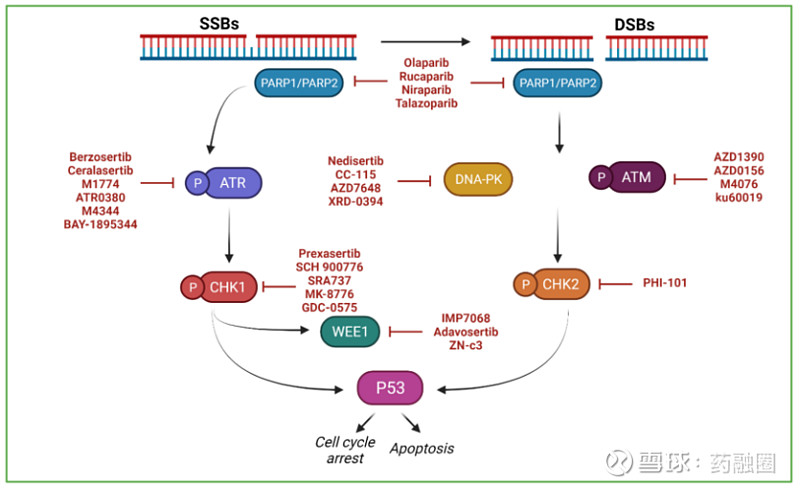
今年AACR大会上出现许多新的合成致死靶点,如PRMT5、Polθ、PLK1、CDK9、PARP7、RAD51、USP1、SMARCA2/4、PKMYT1等。这些新老靶点及其致死搭档整理如下。

小结
PARP的大获成功使得制药公司将目光投向DDR合成致死这一方向,之前拜耳公司(Bayer)在AACR年会上披露ATR抑制剂BAY1895344的数据曾引起轰动。同为DDR通路中的成员,ACCR上的最新数据也验证了,ATR 通路可能是DDR 领域中下一个最有前途的途径。
参考来源:
[1] CDE官网
[2] Synthetic lethality between TP53 and ENDOD1
[3] Polθ inhibitors elicit BRCA-gene synthetic lethality and target PARP inhibitor resistance
[4] BRD4 inhibition induces synthetic lethality in ARID2-deficient hepatocellular
[5] carcinoma by increasing DNA damage
[6] CCNE1 amplification is synthetic lethal with PKMYT1 kinase inhibition
[7] miR-34c-3p targets CDK1 a synthetic lethality partner of KRAS in non-small cell lung cancer
[8]Impact of DNA Damage Response—Targeted Therapies on the Immune Response to Tumours