2023年4月26日, Seres Therapeutics和雀巢健康科学宣布,FDA批准了其粪便微生物疗法 VOWST,用于预防成人艰难梭菌感染(CDI)人群在接受抗生素治疗后的复发,这是首个获批的口服粪便微生物疗法。

VOWST(SER-109)是从人类粪便中纯化的Firmicutes孢子,预计今年6月上市。
2021年7月,雀巢健康科学以3亿美元预付款和里程碑付款与SERES达成协议,在美国和加拿大联合商业化VOWST。
此次获批是基于其III期试验,包括ECOSPOR III和ECOSPOR IV研究。
在ECOSPOR III中,对比安慰剂组的60%,VOWST组88%的人没有复发。(相对风险0.32; 95%[CI], 0.18-0.58)。

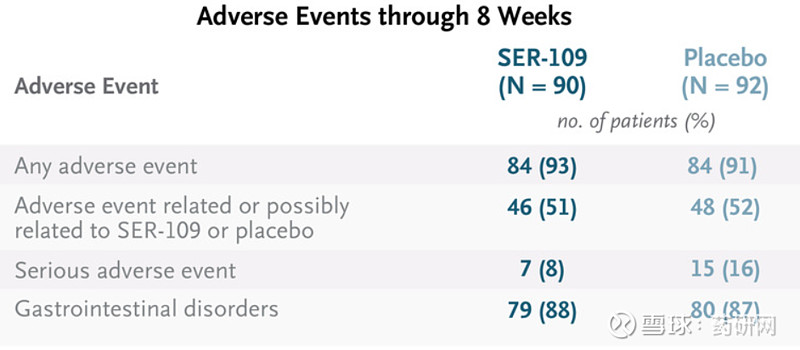
安全性方面,八周内最常见的不良反应是腹胀、疲劳、便秘、寒战和腹泻。
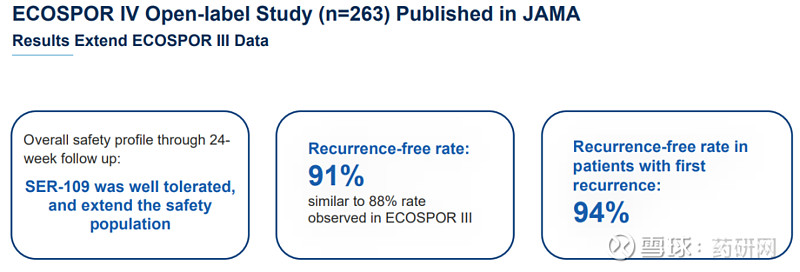
在ECOSPOR IV中,无复发率91%。
复发性CDI(rCDI)代表着重大的未满足需求,是医院获得性感染的主要原因,可能导致严重的疾病和死亡。根据美国疾病控制和预防中心(CDC)的数据,Seres估计2023年美国有15.6万例rCDI。

去年11月30日,FDA批准了首个粪便微生物疗法REBYOTA,同样用于预防rCDI,治疗方式是单剂量直肠给药。
其3期结果显示,在8周内的无复发率为70.6%,而安慰剂为57.5%。

有兴趣相关生物医学领域了解更精彩的内容分享可以关注wechat药研网或雪球药研网。