10月3日,美股上市公司ALX Oncology宣布其ASPEN-06临床试验的预先指定的中期2期阳性数据,一项随机多中心国际研究,评估了该公司的CD47抑制剂evorpacept与曲妥珠单抗、CYRAMZA®(ramucirumab)和紫杉醇联合治疗HER2-阳性胃/胃食管交界处(“GEJ”)癌症患者。这项预先指定的中期分析代表了54名癌症二线和三线胃/胃食管交界处癌症患者的随机结果,包括大量先前接受过ENHERTU®(trastuzumab deruxtecan) 和免疫检查点抑制剂治疗的患者。患者每两周接受一次30 mg/kg的evorpacept治疗,与曲妥珠单抗、CYRAMZA和紫杉醇的治疗周期一致。$康方生物(09926)$ $ALX Oncology(ALXO)$
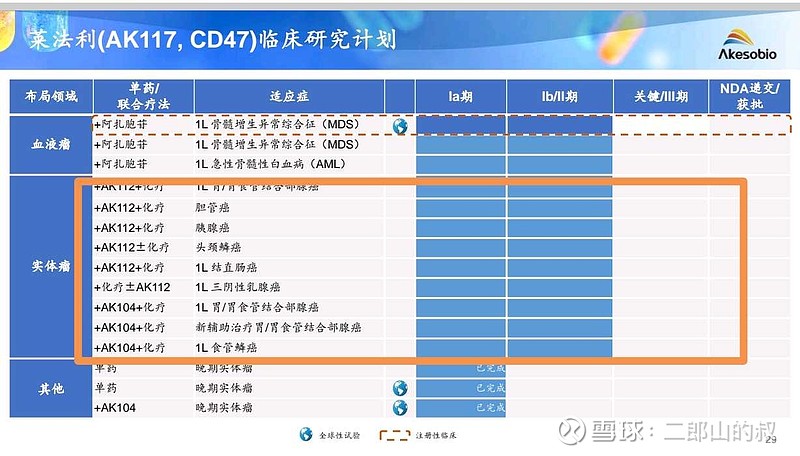
从适应症安排的角度看,ALXO和康方生物都不约而同地在胃癌和头颈鳞癌方面的实体瘤首先着手,康方更是一口气开了4-5个这方面的二期研究,不过都是连用AK112和AK104这两个双抗而中报的时候,夏博士分享的PPT里面是有一业专门介绍了AK117在胃癌和头颈鳞癌的数据,记得是非常不错的,不过康方官网现在挂着的PPT被删除了。
ALXO的ASPEN-06在胃癌和头颈鳞癌的数据同样非常抢眼。
期待CD47在血液瘤和实体瘤都要同步获得突破。