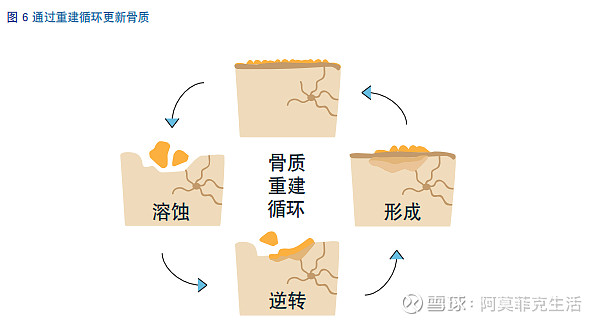
骨骼在人的整个生命中永处于重建状态,整个骨架每10年被更替一次。其 中一组细胞(破骨细胞)被吸引到微 损伤处除去旧骨(骨溶蚀)。一旦破 骨细胞完成任务,形成骨的细胞(成 骨细胞)存人新骨填补缺口。
这个过 程被称为骨重建循环,如图6所示健康 年轻成人骨重建循环。为了保持骨量 恒定,由破骨细胞溶蚀的骨量需要由 成骨细胞形成相等的骨量。
随着男性老化,破骨细胞骨在皮质骨内 表面的溶蚀速度增加(称为内皮质骨溶 蚀)。同时,新骨已被沉积在上皮层的 外表面上(称为骨膜并置)。这些并发的过程的结果是骨的圆周增加,这是用 来增加骨骼体积,让皮质离骨的中心更远。从生物力学的角度看,这两个变化会增加骨强度。
然而,皮质也会变薄, 降低骨强度。所以,在年龄小于70岁 的男性中,这两个进程相互竞争,在一 定程度上保持平衡。
研究表明,绝经后的女性内皮质溶蚀 的速度,骨膜并置无法作为足够的代 偿机制来防止骨脆症。
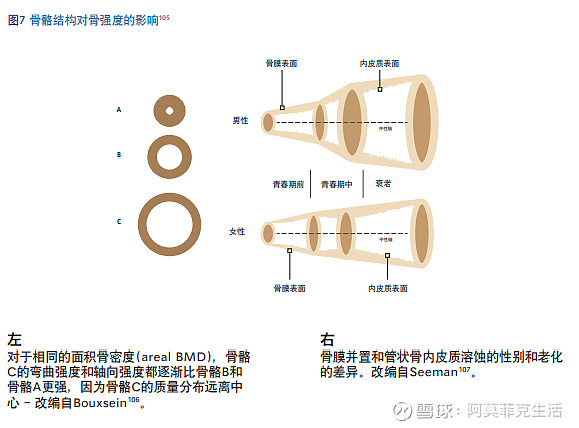
男性和女性随着老化,骨骼截面结构变化如图7 所示。随着老化我们骨骼变化的方式 中所存在的这些看似细微的差别,有助于我们理解为什么女性骨折率在很 大程度上增加的比男性多。
男性与女性差异的另一方面是构成年龄 相关的骨小梁骨质流失的根本机制。 男性出现骨小梁变细,可能与IGF-1降 低有关,而女性出现骨溶蚀和骨小梁 损失,特别是横向的骨小梁损失,可能与绝经期时雌激素缺乏有关。这就是为什么女性骨骼脆性更高的另一个 原因。
70岁以后
随着男性进入老年,重心变为预防和 治疗骨质疏松症,以减少脆性骨折风 险为目标。纵向研究表明,男性70岁 后骨质流失速度加快。随着老化 的进程,骨髓腔的骨质流失没有得到骨膜上骨沉积的补偿,因此造成皮质骨质流失。系统性回顾确立70岁以 上的男性比年轻男性患有脆性骨折的 可能性高出。
正如下一页所显示,骨质疏松症的继 发性原因在男性中非常普遍,最常见 的继发性原因是:
§ 性腺功能低下症
§ 类固醇的使用
§ 过量饮酒
§ 吸烟 性腺功能低下(定义为血清睾酮水平 低于300毫微克/升),调查显示,该情况出现在美国男性护理之家三分之 二遭受髋部骨折的居住者中(见第 13页)。
前列腺癌和骨折
雄激素阻断治疗(ADT)是用于治疗转 移性前列腺癌和老年男性骨质疏松症 显著危险因素的中流砥柱。在第一 年治疗期间,使用ADT治疗的男性骨 质流失是很快,腰椎和髋部的流失速 度为2-4%115,116。
美国对曾在20世纪90 年代被诊断出前列腺癌的50,000多名男 性进行研究,评估骨折的发病率; 接受ADT治疗的男性19.4%骨折,没 有接受ADT治疗的男性12.6%骨折, 相比之下,这在统计学上是显著的差 异(P<0.001)。各种原因的死亡率也 显示接受ADT治疗前列腺癌的男性比 患前立腺癌没有接受ADT治疗或者没 有前列腺癌的男性高。
男性骨质疏松发病原因
常见
§ 库欣综合征或慢性类固醇的使用(>每天5mg,连续使用超过3个月)
§ 过量饮酒(每天超过2个单位)
§ 原发性或继发性性腺功能减退(血清睾酮水平<300ng/dl)
§ 钙的摄取量不足(每天<600mg)
§ 维生素D缺乏或不足
§ 吸烟
§ 家族史(遗传)
较少见
§ 体重指数较低(BMI<20)
§ 缺乏运动或过度运动,导致低体重指数
§ 抗癫痫药(苯妥英钠,苯巴比妥,扑痫酮,卡马西平)
§ 甲状腺毒症
§ 原发性甲状旁腺功能亢进症
§ 1型和2型糖尿病
§ 慢性肝脏或肾脏疾病
§ 吸收不良,包括乳糜泻
§ 高钙尿症
§ 类风湿关节炎或强直性脊柱病
§ 炎症性肠病
§ 恶性肿瘤,例如前列腺癌 » 化疗 » 雄激素阻断治疗
§ 华法林
罕见
§ 多发性骨髓瘤
§ 人类免疫缺陷病毒感染或与蛋白酶抑制剂治疗(替诺福韦)
§ 肥大细胞增多症
§ 免疫抑制治疗(环孢素,他克莫司)
§ 成骨不全症
性腺功能低下(男性睾酮缺乏症) 发生在高达12.3%的男性中,是造成骨质疏松症的显著病因108。 男性性腺功能低下的原因,可以有效地归类为原发性或继发性:
睾丸原发性性腺功能减退缺陷
§ 遗传/染色体疾病(先天性睾丸发育不全综合症XXY)
§ 无睾丸症(先天性或睾丸切除手术后)
§ 隐睾
§ 化疗(烷化剂),放射治疗
§ 睾丸炎(流行性腮腺炎,HIV,自身免疫)
§ 睾丸损伤或扭转
§ 药物(类固醇,秋水仙碱)
§ 酒精
§ 慢性肝脏或肾脏疾病
§ 血色病
下丘脑或垂体继发性性腺功能减退缺陷
§ 特发性:卡尔曼综合征(嗅觉丧失和低促性腺激素性性腺功能减退)
§ 功能性 » 过度运动,体重变化 » 体重指数低 » 全身性或并发疾病
§ 结构性 » 垂体或下丘脑肿瘤,泌乳素瘤 » 浸润(结节病,血色病,组织细胞增生症X,淋巴瘤) » 颅照射,手术,颅脑外伤
§ 药物/医源性 » 雄激素阻断治疗前列腺癌 » 阿片类药物,大麻 » 雄激素外源性管理
在许多国家的全国临床指南中都没有充分地介绍男性骨质疏松症的评估和治疗。骨质疏松症和相关的骨折对世界各地 男性的健康和幸福构成了日益严重的 威胁。国际骨质疏松基金会串联世界 各地全国性患者团体和医药学会一起 呼吁各国政府和医疗专业人员共同努 力,减少骨质疏松症对男性人口的负担。
原文链接:网页链接