精彩内容
根据咸达数据,本周(2018.8.27-9.2)百济神州2款药品提交上市申请;百奥泰生物首家提交阿达木单抗生物类似物的上市申请;东阳光药业又一个1类新药申报临床;海思科医药申报本年度第1个1类化药;此外,小编还整理了本周新提交一致性评价的品种,以及第“六”批通过一致性评价的品种。
| 看点一
百济神州BTK抑制剂BGB-3111提交上市申请,已获CDE承办,受理号CXHS1800023、CXHS1800024。BGB-3111英文名Zanubrutinib,目前提交上市的中文名为赞布替尼,提交制剂为赞布替尼胶囊。
本品是一种小分子抑制剂,靶向BTK(布鲁顿氏酪氨酸激酶),有希望用于治疗多种类型的B细胞相关的淋巴瘤或白血病。
百济神州开发BGB-3111的想法源于公司研发团队对已上市BTK抑制剂伊布替尼的临床数据的研究。团队发现伊布替尼对BTK的抑制并不充分,比如以批准剂量治疗慢性淋巴白血病时,伊布替尼对患者的外周血单核细胞的靶标结合率并未达到100%。于是对药物分子进行改造,使得新的药物分子能够充分抑制BTK的活性,并且对BTK有更高的选择性,同时靶标抑制更为持久。
目前本品在CDE登记的临床试验如下:

此外,8月31日百济神州公司宣布,国家药品监督管理局已受理在研抗PD-1抗体替雷利珠单抗作为治疗复发/难治性经典型霍奇金淋巴瘤患者的新药上市申请,暂时还未进入CDE承办,不过也是双喜临门啊~
| 看点二
百奥泰生物首家提交阿达木单抗生物类似物的上市申请,已获CDE承办,受理号CXSS1800018。这也是国内申报上市的第2个生物类似物,第1个是齐鲁制药的重组抗VEGF人源化单抗注射液(贝伐珠单抗注射液)。
阿达木单抗是一种抗TNF-α单克隆抗体,于2010年首次进入中国,商品名修美乐,批准的适应症包括中度至重度类风湿关节炎以及强直性脊柱炎。本品由艾伯维(Abbvie)公司研发,2017年销售额达到184.27 亿美元,荣升全球销量“6冠王”。然而由于在国内适应症只有2个,且价格略高,因此销售额远不如其他抗TNF-α单抗,国内销售额如下:

(数据来源:咸达数据之信狐药迅)
| 看点三
继上周申报HEC81885对甲苯磺酸盐胶囊之后,本周东阳光药业又一个1类新药申报临床:HEC53856胶囊,已获CDE承办,受理号CXHL1800129、CXHL1800130、CXHL1800131、CXHL1800132。
本品依旧没有更多详细信息披露,小编给大家附送一下本年度截至目前东阳光申报的化药(新药和仿制药)吧:
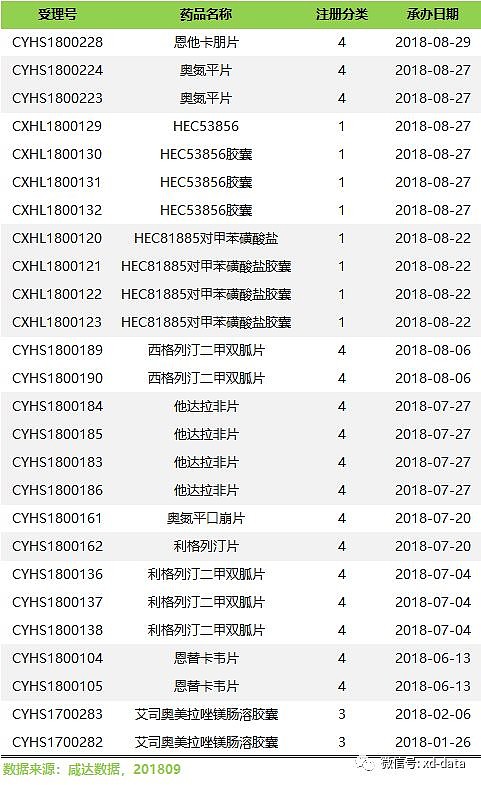
| 看点四
海思科医药申报本年度第1个1类化药:HSK16149胶囊,已获CDE承办,受理号CXHL1800133、CXHL1800134、CXHL1800135。
HSK16149胶囊是由海思科开发的具有自主知识产权的拟用于治疗糖尿病周围神经痛、带状疱疹后神经痛、纤维肌痛的1类新药。临床前研究表明HSK16149具有强效镇痛、长效镇痛、中枢副作用小等特点,HSK16149未来在临床应用中可能具有药效更显著、安全性更好等优势,有望替代普瑞巴林、加巴喷丁,具有成为慢性神经性疼痛首选用药的潜力。
| 看点五
Celgene首次在国内申报1类药品Ozanimod胶囊,已获CDE承办,受理号JXHL1800109、JXHL1800110、JXHL1800111。
本品由Celgene收购Receptos公司获得,是一种口服的第二代S1P1(鞘氨醇-1-磷酸受体1)调节剂。与其他多发性硬化药物相比,该药物在多发性硬化治疗中似乎有效,它可能会带来较少的副作用和毒副反应。此外,本品可能将有效治疗克罗恩病和溃疡性结肠炎,该药物对非特异性溃疡性结肠炎的疗效与阿达木单抗相比大致相同。今年年初,因药理学信息不完整,本品的上市申请被FDA拒绝。期望早日获批上市。
| 看点六
本周又有一大批品种提交一致性评价,此外,第五批通过一致性评价的品种公告(2018年7月26日)之后,又有一些品种通过啦,请注意看!!
第“六”批通过一致性评价的品种如下:
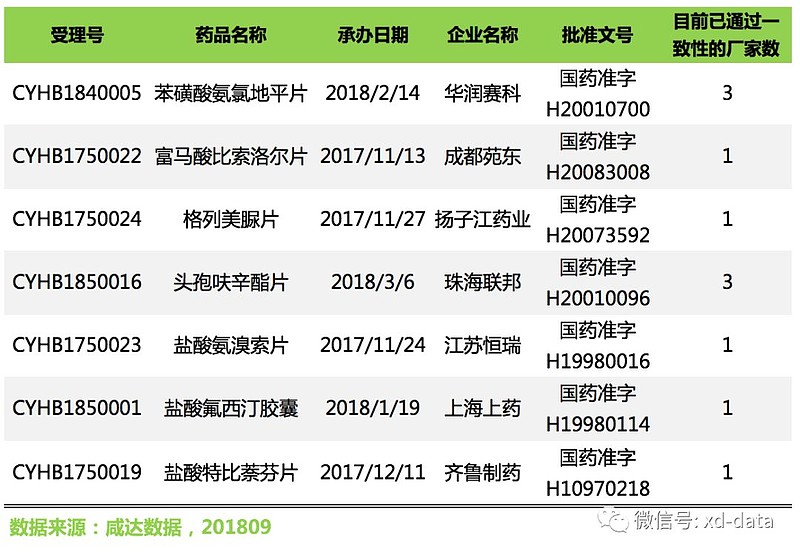
本周提交一致性评价的品种如下:
