精彩内容
根据咸达数据,本周(2018.6.4-6.10)正大天晴提交沙美特罗替卡松粉吸入剂上市申请;4个1类化药审批完毕;3个1类新药和3个1类进口药申报临床;一大批药品提交一致性评价,不乏重磅。
| 看点一
正大天晴药业冲击沙美特罗替卡松粉吸入剂首仿,本周提交4类仿制药上市申请,已获CDE承办,受理号CYHS1700680、CYHS1700681,共计2个规格50μg/100μg和50μg/250μg。
据查,正大天晴在2016年10月登记沙美特罗替卡松粉吸入剂(50μg/250μg)的BE试验,此前还登记过本品的II期临床试验,不过目前看来应该是以BE的数据申报生产。
沙美特罗替卡松粉吸入剂商品名舒利迭,目前国内只有GSK进口上市,共3个规格,正大天晴暂未提交50μg/500μg规格。
舒利迭绝对是个大品种,来感受下其在国内的院内销售额:
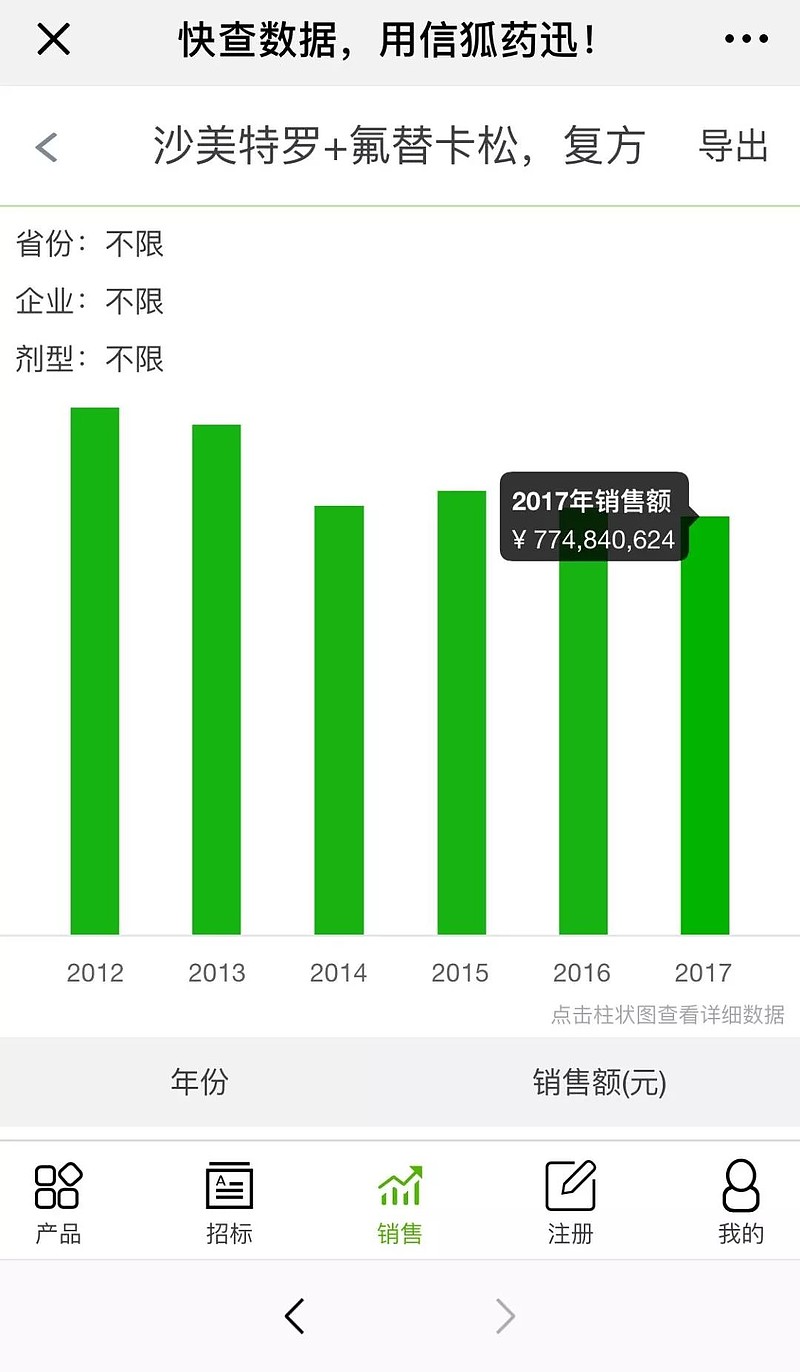
(数据来源:信狐药迅)
| 看点二
本周有4个1类化药审批完毕:
DDCI-01胶囊:本品是重庆文理新药创新团队经过3年多的研究而获得的一种新型磷酸二酯酶5(PDE5)抑制剂,拟用于治疗勃起功能障碍(ED)和肺动脉高压(PAH)。
KL130008胶囊:本品是科伦博泰生物自主研发的小分子JAK抑制剂,治疗类风湿性关节炎。
TG02胶囊和奥卡替尼胶囊暂未查到详细信息,等“通知”!
| 看点三
基石药业/拓石药业联合申报本年度第2个1类化药:CS3001及CS3001片,已获CDE承办,受理号CXHL1700361、CXHL1700362和CXHL1700363。
暂未查到本品的相关信息,基石药业/拓石药业本年度申报的第1个1类化药为MEK抑制剂,目前在国内还在排队待审评。
| 看点四
益方生物申报本年度第2个1类化药:D-0502及D-0502片,已获CDE承办,受理号CXHL1800079、CXHL1800080和CXHL1800081。
据查,本品是一种抗乳腺癌的药物,具体靶点未知,目前已在ClinicalTrial登记临床试验,登记号NCT03471663,这项研究将评估D-0502单药、以及与palbociclib联合疗法治疗晚期或转移性ER阳性和HER2阴性乳腺癌患者的安全性和耐受性。试验计划招募57名受试者,预期的研究开始日期是2018年4月1日,预计的主要完成日期是2020年4月1日。
| 看点五
豪森药业申报本年度第1个1类化药:HS-10340及HS-10340胶囊,已获CDE承办,受理号CXHL1800082、CXHL1800083和CXHL1800084。
暂未查到本品相关信息,豪森的保密工作做的非常好啊!
本周有3个1类进口药首次在国内申报临床:
| 看点六
辉瑞的JAK1抑制剂PF-04965842片申报临床,已获CDE承办,受理号JXHL1800055。
本品是一种每日口服1次的JAK1抑制剂,用于治疗免疫性疾病,目前在ClinicalTrial登记2项3期临床试验,均用于治疗特应性皮炎。
| 看点七
Everest Medicines/Patheon/云济华美药业3家企业联合申报的注射用依拉环素,已获CDE承办,受理号JXHL1800057。
小编推测本品可能就是Ralinepag,代号APD811,是一种用于治疗肺动脉高压的口服新一代选择性前列环素受体激动剂。ralinepag由Arena开发,旨在达到优于目前市面上口服前列环素受体激动剂、与肠外治疗方案相媲美的治疗效果。ralinepag在人体中的药代动力学显示半衰期约为24小时,而且峰谷比较低,每日给药一次即可维持血药浓度。
2017年12月,Arena Pharmaceuticals与Everest Medicines在华签署ralinepag和etrasimod开发及商业化合作协议,Arena将获得2.24亿美元预付款和里程碑付款以及权利金。Everest是一家由康桥资本投资成立的生物制药公司,专注于创新医药产品在中国的开发及商业化。
| 看点八
阿斯利康的BTK抑制剂Acalabrutinib申报临床,已获CDE承办,受理号JXHL1800058。
Acalabrutinib已于2017年11月获FDA批准用于套细胞淋巴瘤(MCL)成人患者二线治疗,为胶囊剂,规格100mg。
| 看点九
本周又有一大批药品提交一致性评价,不乏重磅:
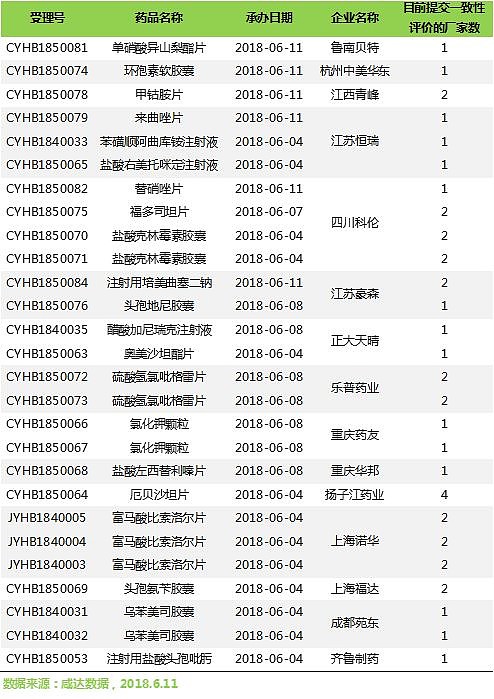
江苏恒瑞一次性提交3个品种的一致性评价,均为首家。信立泰的氯吡格雷已经通过一致性,乐普药业终于也提交了。鲁南贝特的明星产品单硝酸异山梨酯片也提交一致性评价。最后四川科伦同样提交3个产品的一致性评价!