💊 博瑞医药BGM0504口服片剂IND获批深度分析:全球口服双靶点减重药研发里程碑
以下分析基于公开资料及东吴医药团队报告,结合技术壁垒、临床数据、竞争格局及市场潜力展开:
🔬 一、BGM0504口服片剂的核心突破:递送技术赋能口服多肽革命
技术痛点与解决方案
行业瓶颈:多肽类药物口服生物利用度低(如诺和诺德口服司美格鲁肽SNAC技术仅1-2%),限制疗效与成本控制。
奥礼生物Macoral平台:采用甘氨酸二肽+柠檬酸复合物,提升肠道稳定性与渗透效率,目标突破现有生物利用度天花板。该技术有望降低原料成本(减少剂量需求)并改善安全性(减少胃肠道副作用)[^用户提供]。
分子基础优势
BGM0504为GLP-1/GIP双靶点激动剂,其注射剂已证实:
减重疗效碾压替尔泊肽:24周15mg剂量组减重19.78%(安慰剂调整后),显著优于替尔泊肽同剂量组的11.96%。
降糖与安全性:在2型糖尿病Ⅱ期临床中,HbA1c降幅达2.76%,优于司美格鲁肽,且无低血糖事件。
⚡️ 二、研发进度与竞争格局:国内领跑,全球稀缺
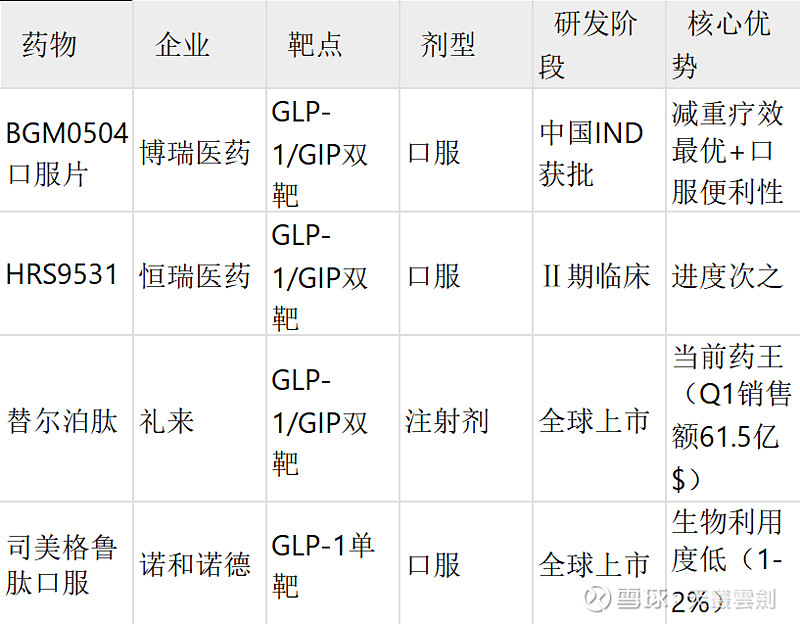
核心结论:
进度领先:博瑞为国内首家推进口服GLP-1/GIP双靶点药物至临床阶段的企业,恒瑞HRS9531片Ⅱ期临床紧随其后[^用户提供]。
疗效潜力:同分子注射剂数据预示口服片剂可能成为减重领域Best-in-class。
💰 三、市场潜力与战略布局:千亿赛道卡位战
GLP-1类药物市场空间
2024年司美格鲁肽销售额破202亿美元(前三季度),替尔泊肽同期110亿美元,双靶点药物增速碾压单靶点。口服剂型因依从性优势,预计将占据减重市场60%份额(弗若斯特沙利文预测)。
博瑞的产能与管线协同
产能储备:2024年规划新增3.5亿支/年BGM0504注射液产能,为口服片剂上市后转化提供基础。
管线协同: BGM1812(长效Amylin类似物):临床前数据显示与GLP-1联用减重效果提升(参考诺和诺德CagriSema方案68周减重22.7%)。 口服复方制剂:探索BGM0504+BGM1812组合,对标MNC巨头下一代疗法。
⚠️ 四、风险提示与催化剂
风险类型详情研发风险口服生物利用度需临床验证;Ⅲ期临床入组进度(当前国内注射剂Ⅲ期进行中)。专利风险欧美专利审查中(中国已授权),需规避礼来替尔泊肽专利壁垒。竞争加剧国内超10家企业布局GLP-1类减重药,信达、华东医药逼近商业化。
近期催化剂:
2025年ADA大会展示BGM0504注射剂Ⅲ期数据(6月)。
BGM1812临床申请(2025下半年预期)。
💎 投资建议:稀缺性技术+临床数据驱动长期价值
博瑞医药凭借口服递送技术突破与双靶点分子设计,有望在千亿减重市场中抢占口服剂型制高点。建议关注:
① BGM0504口服片剂Ⅰ期临床启动(2025Q3);
② 欧美专利授权进展(当前处美国审查尾声);
③ BGM1812临床前数据披露。
风险提示:临床进展、专利挑战及竞品加速。