中国🇨🇳大分子生物药的专利保护范围很窄,只保护#氨基酸序列专利# 。所以,百时美施贵宝(BMS)的PD-1(O药)核心专利(CN101213297B)2026年5月过期。

届时,复宏汉霖、东阳光药、博安生物、迈博药业的O药生物类似药都已经获批上市。
也就是说,与#O药适应症相同的PD-1# ,都会遭到仿制药竞争。
现在,君实生物PD-1卖3万元/年,信达生物PD-1卖3.5万元/年,百济神州PD-1卖5万元/年。
届时O药仿制药可能只卖1万元/年。
(一)胃癌一线适应症会全军覆没,胃癌手术后辅助适应症是幸运星
下雨是PD-1治疗胃癌的中国临床试验进度图。
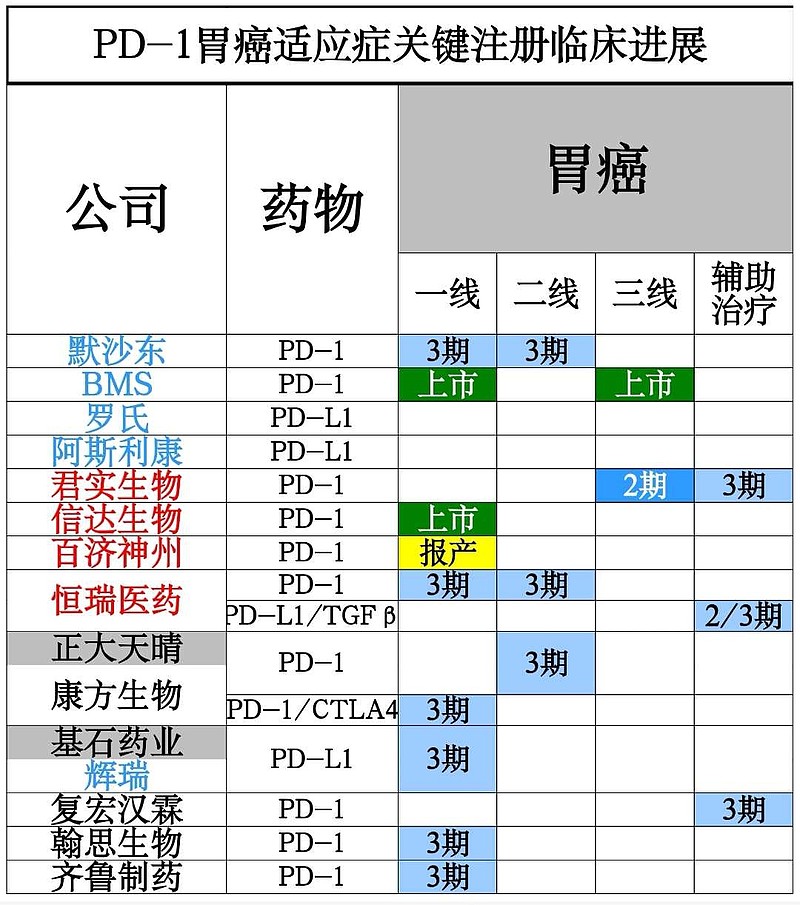
(1)晚期(IVa期、IVb期)胃癌一线
百时美施贵宝的PD-1(O药)一线治疗全人群胃癌,已经在中国🇨🇳获批上市。
$信达生物(01801)$ PD-1胃癌一线获批时间早,也是全人群适应症,还可以分一杯羹。
$百济神州-U(SH688235)$ PD-1胃癌一线,今年达到主要终点,而且仅仅对PD-L1 CPS≥5的亚组患者,有效。根本就没有O药仿制药企的竞争力。
恒瑞医药PD-1、康方生物AK104双抗的胃癌一线治疗,即使获批上市,也只有二年时间的药物生命周期。
君实生物首席医学官很聪明,不开展晚期胃癌一线的3期临床试验,你们信达、百济、恒瑞继续内卷吧。
(2)II期、III期胃癌手术后辅助
2017年美国癌症联合会(AJCC)指南(第八版)将晚期胃癌定义为包括伴有不可切除因素的局部进展期胃癌(Ⅳa)和伴有远处转移的胃癌(Ⅳb),这样的分期与过去只有发生远处转移(M1)才属晚期胃癌(Ⅳ)的理念有所不同,因为其中Ⅳa期在原分期中并不属晚期。因此根据这样的分期标准,晚期胃癌患者的范围更大,包括的患者人群更广。据估计新的分期标准下,晚期胃癌(Ⅳ期)约占中国🇨🇳胃癌患者的40%。
换一句话来说,大部分胃癌患者(60%比例),其实需要手术后PD-1辅助治疗。
百时美施贵宝的O药,也于2020年开展了III期胃癌(包括胃腺癌)的手术后辅助亚洲多中心3期临床试验。

$君实生物-U(SH688180)$ 的特瑞普利单抗(PD-1)也于2021年开展了II期和III期胃腺癌的手术后辅助#国际多中心3期临床# 。适应症范围更广,无惧O药仿制药竞争。
曰本、韩国新增胃癌,大多数是早期胃癌,适合于手术后PD-1辅助治疗。
而不是选择——晚期胃癌一线治疗。
(二)非小细胞肺癌手术后PD-1辅助治疗
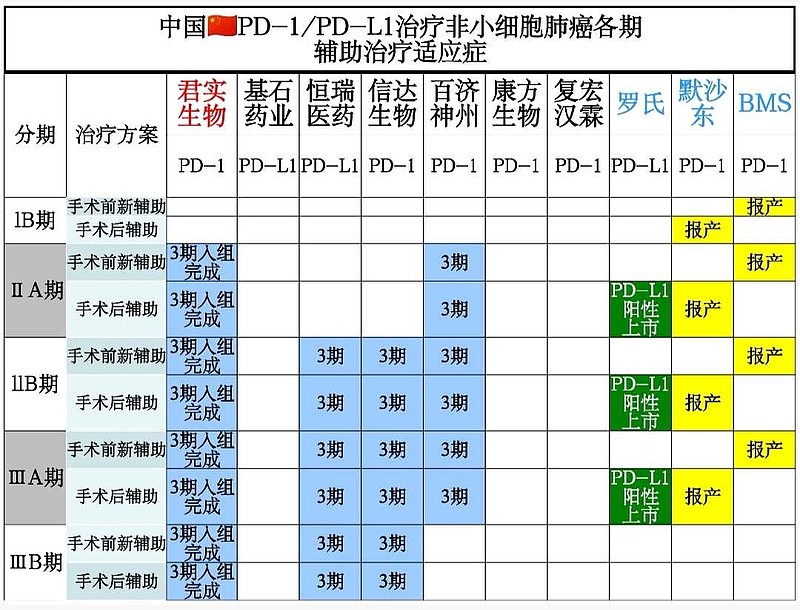
百时美施贵宝O药,仅仅只有非小细胞肺癌手术前新辅助,将获批上市。
君实生物PD-1非小细胞肺癌围手术期辅助治疗3期临床,今年就要完成入组数据读出啦,中国进度第一。
信达生物PD-1,竟然去年才开展非小细胞肺癌围手术期辅助治疗3期临床,考虑到国际多中心研究进度会更慢,比君实生物进度整整慢了4年时间。
(三)O药可能提前数年大幅降价
由于百时美施贵宝的O药在中国太贵(11万元/年),一年销售额仅仅2+亿元。
去年,恒瑞医药卖了41亿元,信达生物PD-1卖了31亿元,百济神州PD-1卖了16亿元。
你们猜猜,百时美施贵宝会不会大幅降价,用于占领食管鳞癌、食管腺癌、胃癌一线的PD-1中国市场?

@今日话题 @水里望月 @生煎只爱大壶春 @招财小黄鸭 @柳叶刀找脊梁 @北京栗男 @大个的鼹鼠