6 月 10 日,NMPA 官网显示,恒瑞 3 类仿制药「阿齐沙坦片」获批上市并视同通过一致性评价,成为国内首仿。

阿齐沙坦(azilsartan)是武田制药开发的新一代选择性 AT1 亚型血管紧张素 II 受体拮抗剂(ARBs)类抗高血压药,通过与血管紧张素 II 受体结合发挥拮抗血管紧张素 II 的作用,从而抑制血管收缩,降低末梢血管紧张度,以达到降压作用。
阿齐沙坦最早由日本武田制药公司研发,于 2012 年 1 月日本获批,以「Azilva」为名上市。该公司 2016 年年报显示,Azilva 及其系列产品将在 2016-2018 年帮助公司引领日本制药市场。分析师认为该药销量还将继续保持增长,2022年销售额约为7.49亿美元。目前,阿齐沙坦核心专利已到期,原研尚未在国内上市。
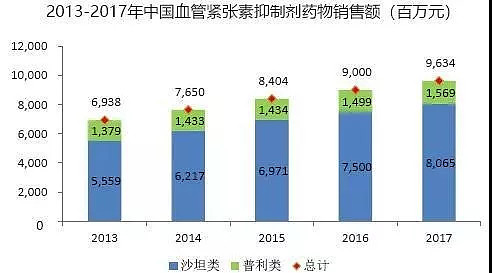
据了解,2017 年血管紧张素抑制剂类药物在中国总销售额为 96 亿元;其中沙坦类销售占比为 83.7%,目前国内有依普沙坦、坎地沙坦酯片、厄贝沙坦、奥美沙坦、缬沙坦等 17 个单方或复方的沙坦类药物,2017 年坎地沙坦酯的销售总额为 6.24 亿,在沙坦类的销售额占比为 7.7%。阿齐沙坦是坎地沙坦酯的二代产品,阿齐沙坦在降压效果和降压平稳性方面更优,安全性与坎地沙坦酯相当,销量有望超过坎地沙坦酯。
Insight 数据库 显示,截止 2021 年 5 月,国内阿齐沙坦片在研企业有 59 家。除本次获批的恒瑞之外,扬子江药业、兆科药业等 4 家企业处于上市申请中,山东新时代、瑞阳制药、科兴药业等 5 家企业处于 BE 试验中,另外东阳光、先声药业、成都倍特等 48 家药企拿到临床批件未启动临床试验。
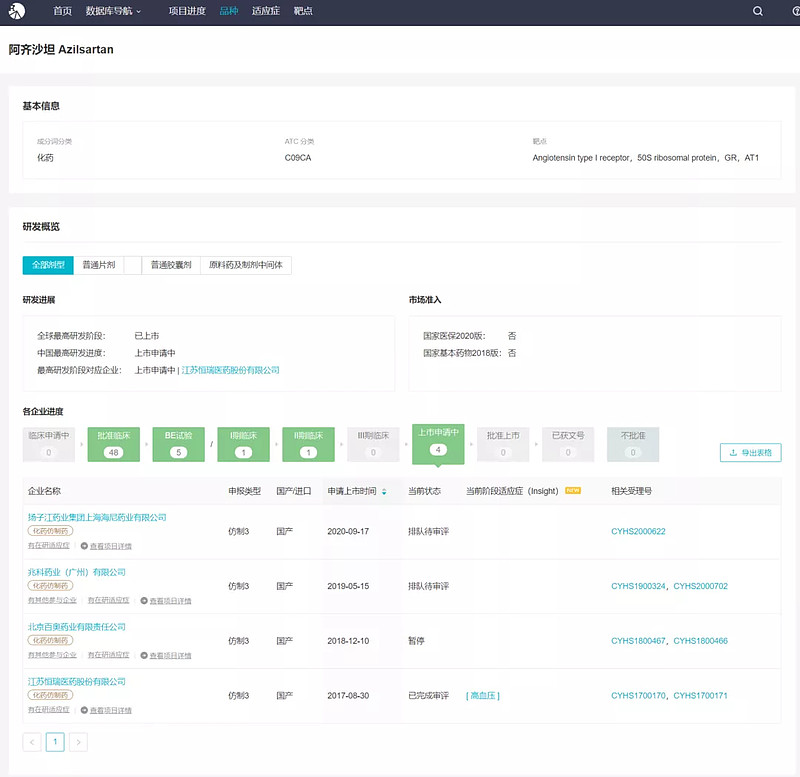
来自:Insight 数据库(网页链接)
上市申请第一梯队中,兆科药业和百奥药业紧随恒瑞之后。
恒瑞于 2012 年开始向 NMPA 申请临床批文,2014 年 9 月 9 日获批临床,2017 年 6 月 15 日提交上市申请获受理,2017 年 12 月 18 日以「专利到期前 1 年的药品生产申请」为由纳入优先审评,今日正式获批。
据恒瑞 2018 年报显示,截至 2018 年底,恒瑞阿齐沙坦片研发项目已投入研发费用研发费用 988 万人民币左右。阿齐沙坦获批上市后,恒瑞获得了继奥美沙坦酯、厄贝沙坦片之后的第 3 款的沙坦类药物。