$双鹭药业(SZ002038)$ 奥硝唑注射液申请一致性评价注册已经受理,由于生产工艺较高,具有技术壁垒,预测将是国内独家通过奥硝唑注射剂一致性评价注册的药企。
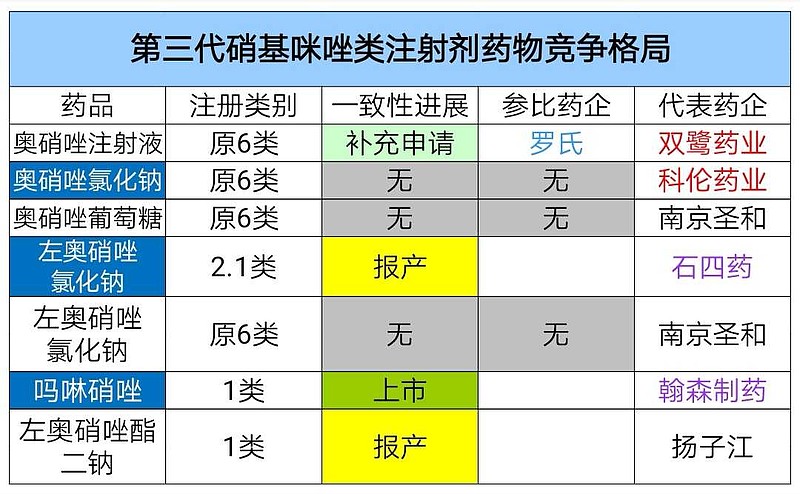
既往的医保目录内,奥硝唑注射液,奥硝唑氯化钠,奥硝唑葡萄糖,左奥硝唑注射液都是可以医保支付的品种。 奥硝唑(注射剂)每年国内终端市场规模26亿元。双鹭药业独家通过一致性评价之后,即使只取得国内50%市场份额,每年也有13亿元营收。


根据万隆制药《2018年招股说明书》,科伦药业占有硝基咪唑类药物最大市场份额。 其中,奥硝唑注射剂型(包括奥硝唑注射液、奥硝唑氯化钠、奥硝唑葡萄糖三种类别)市场销售额是26亿元。
2017年12月22日,CDE发布的《已上市化学仿制药(注射剂)一致性评价技术要求》,对注射剂一致性评价作出了明确要求。 根据要求,注射剂仿制药做一致性评价在选择参比制剂时,首选国内上市的原研药品;如原研药品国内未上市,应选择欧美日已上市的原研药品(对于多个国家/地区的,建议依次选择在美国、欧盟和日本已批准上市的)。如果原研药品在国外上市的处方不一致,申请人按照现有技术要求进行评估,选择更合理的原研药品。
本文中以奥硝唑注射液的罗氏原研药(Tiberal®)和双鹭药业的仿制药(遁宁®),来看看怎样才是真正的一致性评价。

(一致性注册辅料要求)
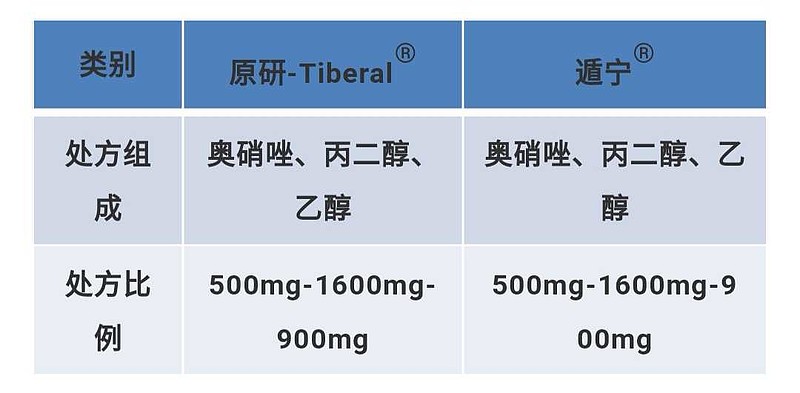
由以上数据可见,双鹭药业的遁宁®处方组成与比例,均和原研药Tiberal®相同,符合上述注射剂仿制药一致性评价中辅料种类和用量通常应与参比制剂相同的要求。
国内大多数仿制药企使用的奥硝唑、左奥硝唑水溶性极差,传统厂商通常采取加入大量的酸来增强药物水溶性。但是由于大量酸的加入,使得溶液pH值偏低(做成输液制剂时pH在3.5左右而人体耐受pH为4.0~9.0),易产生静脉炎。并且输液高温灭菌时毒性降解产物2-甲基-5硝基咪唑较高,给临床用药带来较大的不安全。

(一致性注册PH值和内毒素要求)
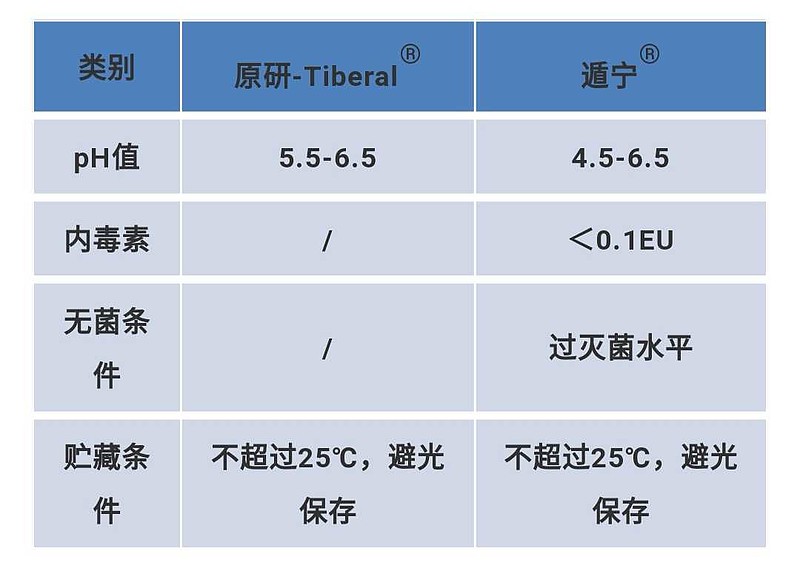
由以上数据可见,双鹭药业的遁宁®在ph值、内毒素、无菌条件、贮藏条件方面,与原研药Tiberal®基本一致。

(一致性注册规格要求)
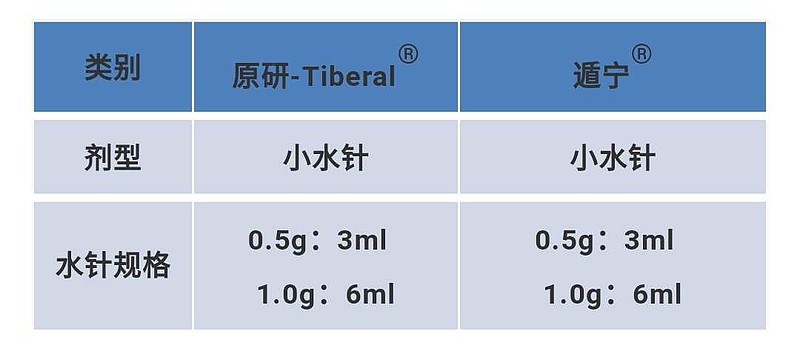
双鹭药业的遁宁®的剂型和规格,与原研药Tiberal®完全一致,是目前唯一符合一致性评价要求的奥硝唑注射液。
目前为止,市场份额最大的科伦药业和万隆制药都是奥硝唑大输液。根本不符合一致性评价最简单的要求。

目前内地其他奥硝唑注射剂仿制药都建议儿童慎用,不建议三岁以下儿童使用,原研Tiberal®临床却可用于儿童。 在此基础上,双鹭药业的遁宁®与原研一致,说明书有着完整的儿童用药信息,更加规范指导临床儿童、新生儿和婴儿需要用药,确保用药有据可循和安全。
也就是说,面对26亿元内地大市场,科伦药业等内地药企没有突破奥硝唑注射剂生产工艺壁垒,无法完成一致性评价注册。即使科伦药业等未来试图绕开相关技术限制,也需要按照新4类或者新2类重新报产,至少需要>3年时间才能上市竞争。