创新药PK的下一个战场
得益于药政改革、技术红利和资本投入,中国创新药发展态势持续向好。自2016年以来,国家药品管理局已批准了近200款创新药。与此同时,还有数百个创新药正处在临床开发的中后期,有望在未来几年陆续上市。医药魔方数据显示,国内创新药项目在靶点和适应症方面集中度较高,以VEGF/VEGFR、PD-1/PD-L1、CD19、HER2等靶点为代表的临床项目高达数百个,且大多集中在肿瘤适应症。
创新药靶点扎堆令人喜忧参半。喜的一点在于,多数靶点多为fast follow,成药性相对确切,待它们大量上市后,可以预期到价格会下降,提高中国肿瘤患者在创新药使用上的可及性。忧的一点则是,未来众多同质化产品在存量市场“拼低价”的模式能否让创新生态可持续?以及医生/患者面对同类型产品究竟该如何选择?在此背景下,便有行业人士疾呼,真实世界研究(Real World Study,RWS)或成为创新药“出圈”的途径之一,是创新药PK的下一个战场。
元年开启
有人将2020年比作“中国真实世界研究的元年”,因为国家药监局2020年1号文颁给了“真实世界”。2020年1月,国家药监局药品审评中心(CDE)发布《真实世界证据支持药物研发与审评的指导原则(试行)》(下称《指导原则》),这是继2019年5月CDE发布《真实世界证据支持药物研发的基本考虑(征求意见稿)》(下称《征求意见稿》)后,对真实世界证据(Real World Evidence,RWE)支持药物研发和上市规则的进一步明确和细化,并明确了RWE在药物监管决策中的地位和适用范围,该原则的颁布被业界评为“里程碑事件”,RWS在行业引发的讨论和关注度也越来越热。
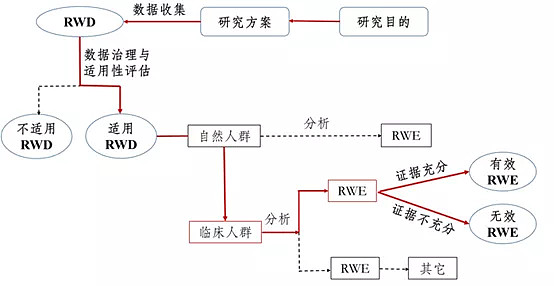
支持药物监管决策的RWS路径(实线所示)
RWS起源于实用性的临床试验,是在较大样本量基础上,根据患者的实际病情和意愿选择治疗措施,并开展长期评价。按照CDE定义,真实世界数据(Real World Data,RWD)是RWS的基础,前者包括与患者使用药物以及健康状况有关的和/或来源于各种日常医疗过程所收集的数据。RWD经过分析后能用于支持药物上市研究的证据便是RWE。
RWE的概念最早可以追溯到2016年12月奥巴马签署《21世纪治愈法案》,经过5年多的发展,RWD用于RWS的指导规范逐步清晰、RWE支持药品研发和审评决策的政策法规逐步明朗。根据《指导原则》,RWE的主要用途包括5方面:
为新药注册安全性和有效性证据;
提供现有药品标签变更证据;
上市后安全性和有效性评估;
研发传统中药制剂;
用于支持监管决策的其他用途。
在创新药未上市之前,药企通过随机对照试验(RCT)证明“与安慰剂相比,XX药疗效显著”。随着中国创新药的大力发展催生更多的创新药上市,创新药之间的竞争加剧。比如说目前PD-1/L1领域,目前有数十家产品在该领域发力,企业或需要通过RWS结果强调“XX药较YY药,疗效更显著”,以显示自家产品较竞品的优势。创新药采用RWS,除了强调较竞品的优势,还有可能在临床实践的超适应证用药的情况下,收集并分析这些数据可探究药物在尚未获批的疾病及人群中的疗效,进而为上市后药物扩大适应证提供可能。今年4月,FDA批准了Ibrance(哌柏西利)新适应症的补充申请,联合一种芳香酶抑制剂或者氟维司群用于治疗男性HR+、HER2-晚期或转移性乳腺癌。此次批准也是FDA基于真实世界用药数据。