本周,受美股Intercept公司的奥贝胆酸(obeticholic acid,OCA)非酒精性脂肪肝炎(Non-alcoholic steatohepatitis,NASH)适应症REGENERATE关键临床3期试验的新中期分析结果积极,获批概率上升影响,美股NASH相关研发公司股价全线高涨,显示出市场对于NASH产品上市前景的乐观情绪。
NASH是由肝脏中脂肪堆积引起的肝脏疾病和炎症,市场巨大。目前对于NASH尚未有确切的病因指向,这类患者通常伴有肥胖;目前病因指向上大概有肥胖、II型糖尿病、高胆固醇血症、胰岛素抵抗以及代谢综合征等。根据流行病学数据,全球酒精性脂肪肝病(non-alcoholic fatty liver disease,NAFLD)发病率约25%,这些患者约有10-20%的可能进展为NASH,全球各地NASH发病率约为1.5%至6.5%,中国约为3.5%(即目前美国NASH患者人数约为1500-3000万,中国约有5000万NASH患者),有三分之一的NASH患者合并2型糖尿病,并且NASH可能为成为未来10年患病人数最多的慢性肝脏疾病。虽然目前NASH存在巨量的患者群体,但受限于NASH发病机理的复杂,目前FDA未批准任何适应症为NASH的药物或治疗方案。
尽管目前还没有获得FDA批准的治疗方法,但目前多种有前途的药物正在临床开发中用于治疗NASH,其中包括许多处于2期或3期临床开发阶段的研究。目前,NASH相关注册试验共400项(美国临床试验数据库354项,中国临床试验注册中心21项,国家药品监督管理局药品审评中心25项)。
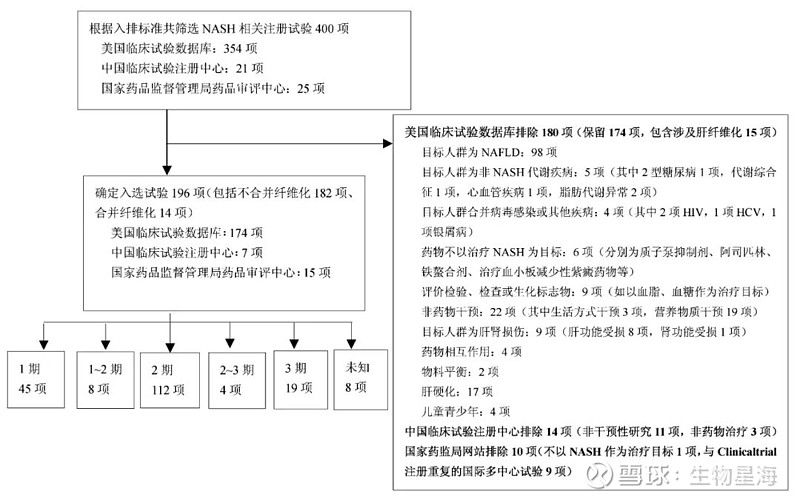
数据来源:临床肝胆病杂志
近年来,NASH药物的研发处于快速增长阶段。NASH药物临床研究始于2000年后,2001年—2005年共有9项,2006年—2010年共17项,2011年—2015年共32项,2016年—2020年共105项,2021年到2021年8月为止共33项,注册数量呈递增趋势。目前,处于临床后期的NASH在研药物主要包括Intercept公司的奥贝胆酸、Inventiva公司的Lanifibranor、Madrigal公司的Resmetirom、诺和诺德的索马鲁肽、Galmed的Aramchol等。其中Intercept的奥贝胆酸与Madrigal的Resmetirom是最被市场所看好的药物。造成近年来NASH药物研发火热的一大原因是FDA对于NASH药物审评标准的变化。2018年12月与2019年6月,FDA连续出台了两份NASH研发指南草案,涵盖了从动物模型的选择到后期临床试验的规划、3期临床试验的患者招募、临床终点、以及安全性考量等多个方面。

数据来源:临床肝胆病杂志
国外NASH新药的火热研发必将带动产业上下游蓬勃发展。目前,我国本土NASH临床新药相对较少,泛磷酸二酯酶(PDE)抑制剂ZSP601是国内首个获批NASH临床的首创新药。相对于药物研发,NASH相关诊疗器械同样值得关注。
从NASH临床试验端看,影像学等评价方法越来越得到重视,相关设备具备投资机会。对于目前NASH的临床入组,主要的评估方法包括:病理评分,主要以NAS评分和NASH-CRN病理评分的分级为标准;影像学评估,主要为Fibroscan、MRI质子密度脂肪分数(MRI-PDFF)、磁共振弹性成像(MRE)等;BMI和体质量变化。综合来看,在临床试验端,NASH的诊断仍以病理作为金标准,但是随着对NASH认识的增加,以及临床试验数据的支持,MRI-PDFF、MRE、Fibroscan等无创影像学手段在相对早期阶段的NASH试验的地位逐渐提升,而且作为金标准的病理诊断,可能存在较大的组间和组内诊断差异,但对于确证性试验,病理仍作为最重要的入选和疗效标准。
而从临床实际端看,由于活检存在患者依从性较差、风险较大等问题,影像学与血液学检测相结合的诊断方法,将发挥越来越大的作用。
可以预见,未来随着NASH药物研发的继续推进,以及若NASH新药成功上市,必然带来NASH相关药物及诊疗的蓬勃发展,带来相关诊疗仪器的巨大需求。
重点关注公司
消费医疗重点关注福瑞股份(软肝片与NASH诊疗仪器的海外龙头)、迈瑞医疗(诊断设备龙头)、众生药业(NASH药物研发);华润三九(OTC总龙头)、长春高新(对集采的预期消化,医美概念,估值修复)和正海生物(齿科高成长赛道,新增生物活性股等新产品);互联网药店与线下药店,四大药房率先反弹,关注低位股补涨;同时关注京东健康和阿里健康(同样受益处方外流,打压平台经济和3P业务的悲观预期已体现);品牌中药关注达仁堂(高股权激励预期)、寿仙谷(灵芝孢子粉等省外扩张)和以岭药业(中药创新龙头)等。
创新药关注全球化同步发展的药企,如百济神州、恒瑞医药、信达生物、荣昌生物、康方生物、信立泰、泽璟制药、海创药业和复宏汉霖等;创新器械出海重点关注新产业、微创医疗、南微医学等;进口替代关注海泰新光、澳华内镜、启明医疗和心通医疗等。
其他重点关注:原料药和CXO,金城医药、成都先导、博瑞医药和键凯科技等。
风险提示:国内疫情进程的不确定性风险、国际环境剧烈变化的风险等。