有观点,有态度
这是医业观察的第2092-5期文章
来源:艾德生物
近日,由中国医师协会医学技师委员会病理技术专家组等多个学会共同撰写的《微卫星不稳定性(MSI)检测技术专家共识》(以下简称“共识”),在《临床与实验病理学杂志》上发布,这是我国第一个从检测技术维度撰写的MSI专家共识。

向左滑动查看具体内容

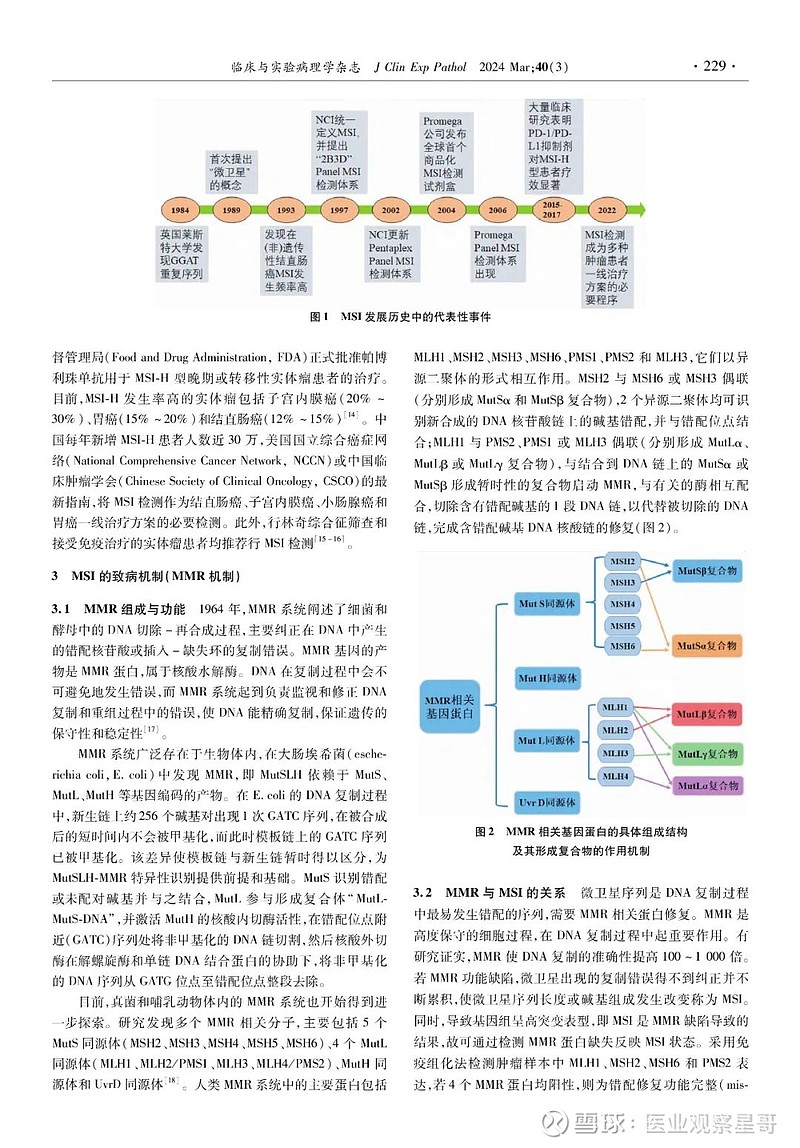





《微卫星不稳定性(MSI)检测技术专家共识》原文[1]
共识从MSI的定义、发展历史、致病机制、临床意义、检测方法、样本的选择与要求、质控、结果判读和报告规范等方面进行了全方位的论述。共识指出,MSI在结直肠癌、胃癌、子宫内膜癌等多种实体瘤中高发,进行MSI检测可以辅助筛查林奇综合征,帮助结直肠癌患者进行5-FU类化疗药物选择,对结直肠癌、胃癌和小肠腺癌患者进行预后分层,以及预估多种实体瘤免疫检查点抑制剂的治疗获益。
2023年11月,艾德生物的人类微卫星不稳定性(MSI)检测试剂盒(国械注准20233401589)获得国家药监局批准,用于检测实体瘤患者MSI状态,检测结果可用于替雷利珠单抗的伴随诊断,并实现了三个“首个”:我国首个泛癌种免疫治疗伴随诊断检测试剂盒、首个MSI伴随诊断检测试剂盒,以及首个同步开发伴随诊断检测试剂盒。艾德生物MSI检测试剂盒全面满足实体瘤患者在不同诊疗时机的检测需求,让肿瘤患者真正从精准诊疗中获益。
参考文献
1.《临床与实验病理学杂志》,J Clin Exp Pathol 2023 Mar;40(3),doi: 10.13315/j. cnki. cjcep. 2024. 03. 002
▍关于艾德生物
厦门艾德生物医药科技股份有限公司(股票代码:300685)聚焦在肿瘤精准医疗分子诊断领域,专注于科技惠民的技术创新,致力为患者提供合规、高品质的诊断产品和服务,让患者从精准医疗中真正获益。公司拥有国家企业技术中心、工信部专精特新小巨人企业、博士后科研工作站、发改委基因检测技术应用示范中心、国家高新技术企业、福建省肿瘤高通量测序工程研究中心等资质,GMP标准厂房获得国家药监局(NMPA)和欧盟ISO13485资质认证;公司拥有ADx-ARMS®、Super-ARMS®、ddCapture®、ADx-HANDLE®等核心技术,核心技术获得中国、美国、欧盟、日本专利授权,荣获国家科学技术进步奖二等奖、中国专利奖银奖;公司产品覆盖具备精准医疗条件的各大癌种,除了在国内三甲医院大规模应用外,部分产品在日本、韩国获批上市并进入当地医保,开创了我国肿瘤伴随诊断海外获批的先例。公司下设厦门艾德医学检验实验室、上海厦维医学检验实验室,拥有医疗机构执业许可证、通过美国病理学会(CAP)认证和ISO15189认可。目前全球数十个国家和地区的客户选择了艾德产品和服务,每年有数十万肿瘤患者从中受益。公司瞄准行业创新源头,以伴随诊断赋能原研药物临床,是众多顶级药企肿瘤药物开发的战略合作伙伴,是国际知名的民族品牌。
---The End---
欢迎扫码添加医业观察星哥微信号
欢迎点击关注
喜欢就一键三连,点赞,在看,分享!