Chroma Medicine日前宣布其表观遗传编辑平台在体内(in vivo)靶向包含PCSK9在内两个不同靶点的效力,数据显示此平台沉默99%靶点表达,成功完成概念性验证。详细数据在今年美国基因和细胞治疗学会(ASGCT)第26届年会上公布。

PCSK9是降低低密度脂蛋白胆固醇(LDL-C)的一个重要靶点,目前已经有多款靶向PCSK9的抗体疗法和一款RNAi疗法获批上市。PCSK9蛋白的作用是抑制LDL受体的回收和再利用。因此,降低PCSK9蛋白的水平可以让更多LDL受体回到肝细胞表面,与更多LDL结合,将它们从血液中清除。
Chroma的表观遗传编辑系统将DNA结合结构域与表观遗传效应结构域偶联,其中DNA结合域特异性地靶向需要沉默或激活的单个或多个基因,效应结构域则负责调控DNA的甲基化模式,控制染色质构象,并激活或抑制基因表达。这种方法不需切割DNA序列、或激活结果难以预测的DNA修复通路,避免因切割DNA序列产生的潜在副作用。
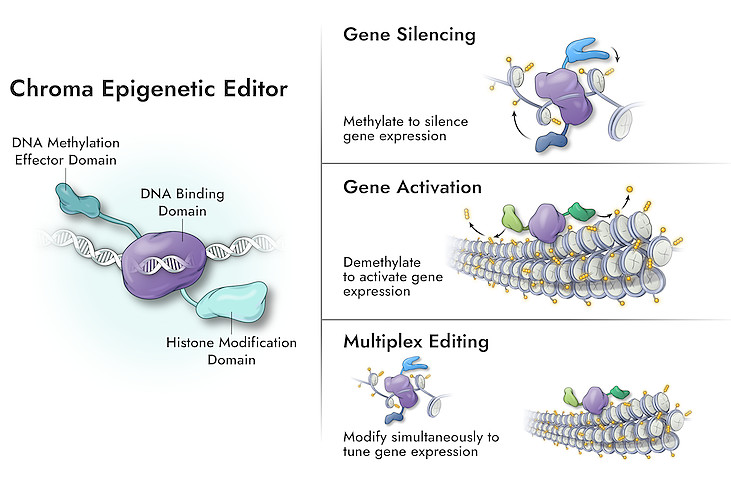
▲Chroma的模块化表观遗传编辑工具可以持久地开启或关闭基因,或同时改变几个基因的表达(图片来源:Chroma公司官网)
这次所公布的研究展现Chroma所开发PCSK9靶向表观遗传编辑器的作用。数据显示,其表观遗传编辑器在转基因小鼠中展示出高效、持久且具特异性的PCSK9沉默。在观察至少五个月的情况下,Chroma的表观遗传编辑器经过一次剂量的应用后,观察到了PCSK9沉默达99%,没有检测到基因表达或甲基化的脱靶作用。
此外,Chroma数据也显示其表观遗传编辑器具广泛应用和模块化的潜力。数据显示,将靶向PCSK9的指导RNA(gRNA)替换为靶向HBV基因组的gRNA时,可以在转基因HBV小鼠模型中通过一次给药产生强效且持久降低乙型肝炎表面抗原(HBsAg)至低于定量下限的效果。

▲Catherine Stehman-Breen博士在2023药明康德全球论坛上对细胞和基因疗法的治愈潜力充满期待
Chroma的首席执行官Catherine Stehman-Breen博士在参加2023年药明康德全球论坛时提出实现细胞和基因疗法成为产业未来主流的关键在提高疗法的安全性以及对医生和患者进行教育,“帮助他们理解什么是细胞和基因疗法,它们如何运作等。”Chroma表观遗传编辑器的高效力与创新性更是强化此一观点的重要性。
根据新闻稿,这些实验结果显示表观遗传编辑是潜在进行基因调节的模式,Chroma预计将在即将到来的科学会议上展示更多数据。
参考资料:
[1] Chroma Medicine Presents Data Demonstrating Near-Complete, Durable In Vivo Silencing with Targeted Epigenetic Editors at 2023 ASGCT Annual Meeting. Retrieved May 19, 2023 from 网页链接
@药明康德 内容团队编辑
本文来自药明康德内容团队,欢迎转发,谢绝转载到其他平台。
免责声明:药明康德内容团队专注介绍全球生物医药健康研究进展。本文仅作信息交流之目的,文中观点不代表药明康德立场,亦不代表药明康德支持或反对文中观点。本文也不是治疗方案推荐。如需获得治疗方案指导,请前往正规医院就诊。
⤵️喜欢我们的内容,欢迎关注@药明在线 ,或者点赞、分享给其他读者吧!