7月18日,NMPA发布公告决定对西达本胺说明书【不良反应】【注意事项】进行修订。
【不良反应】项和【注意事项】的“特别注意事项”下增加以下内容:
上市后监测到心力衰竭和间质性肺炎的不良事件报告,发生率不明,相关性尚无法排除。
西达本胺2014年获NMPA批准用于既往至少接受过一次全身化疗的复发或难治的外周T细胞淋巴瘤(PTCL)患者。2017年7月作为36种谈判药品纳入《国家基本医疗保险、工伤保险和生育保险药品目录(2017年版)》乙类范围,支付标准为385元(5mg/片)。
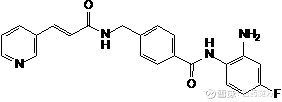
西达本胺结构式
西达本胺是由微芯生物自主研发的国际上首个亚型选择性组蛋白去乙酰化酶(HDAC)口服抑制剂,是一种具有全球专利保护的全新分子体,是国家“863”、十一五及十二五“重大新药创制”专项课题。西达本胺为苯酰胺类HDAC亚型选择性抑制剂,主要针对第I类HDAC中的1、2、3亚型和第IIb类的10亚型, 具有对肿瘤异常表观遗传功能的调控作用,通过抑制相关HDAC亚型以增加染色质组蛋白的乙酰化水平来引发染色质重塑,并由此产生针对肿瘤发生的多条信号传递通路基因表达的改变。
此外,单药及联合其他抗肿瘤药物针对弥漫性大B细胞淋巴瘤、非小细胞肺癌、乳腺癌及HIV的临床研究在多个国家和地区开展。今年5月,江泽飞教授在柳叶刀肿瘤杂志发表一项西达本胺联合依西美坦治疗晚期HR+乳腺癌的III期临床积极结果。
西达本胺上市后推动了微芯生物业绩快速增长,2016年、2017年和2018年,西达本胺片的产品销售收入和西达本胺境外专利授权许可收入的合计分别为8,529.96万元、11,028.87万元和14,651.14万元,占公司同期营业收入的比例分别为99.92%、99.81%和99.20%。这次微芯生物能成为科创版医药第一股,西达本胺可以称为一大功臣。