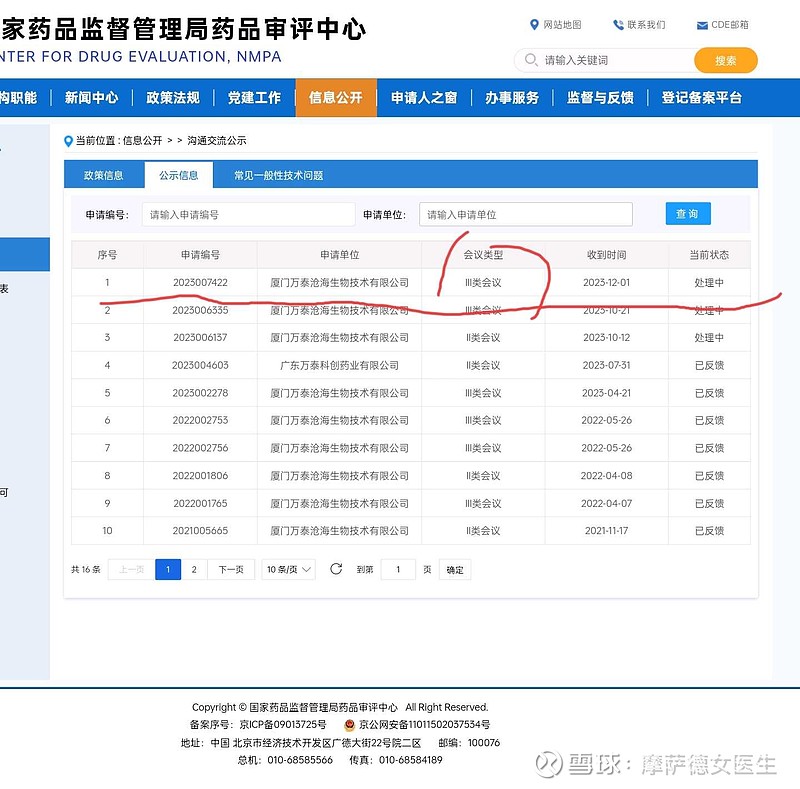
2024年上市,应该没问题。$万泰生物(SH603392)$
| 发布于: 修改于: | Android | 转发:2 | 回复:28 | 喜欢:3 |

2024年上市,应该没问题。$万泰生物(SH603392)$
3、Ⅲ类会议,系指对创新药物召开的除Ⅰ类和Ⅱ类会议之外的其他会议。
可以看出,I类会议主要用于研发过程中,也是临床过程中的重大事件,对受试者和产品本身都可能带来巨大隐患和伤害。Ⅱ类会议贯穿整个产品临床研究以及批准上市后的风险控制。其他类型的问题沟通,则属于Ⅲ类会议。
同时《办法》还明确了申报时间以及申报资料要求和流程。Ⅰ类会议在提出会议申请后30天内召开;Ⅱ类会议在提出后60天内召开;Ⅲ类会议在提出申请后75天内召开。当然,审评中心在召开之前会和申办方提前沟通,如果沟通过程中已经把问题解决,会议可以取消。会后形成的会议纪要需要双方签字并且作为申报资料,也是审评依据。
可以说,新的《办法》让申请人有一个明确和规范的渠道,提供自己的诉求,也体现出药品审评中心对于申请人以及整个行业开放的态度。说明我国药品审评改革中公开透明的宗旨。
三类会议,预示着离批准上市不远了,$万泰生物(SH603392)$
3、Ⅲ类会议,系指对创新药物召开的除Ⅰ类和Ⅱ类会议之外的其他会议。
可以看出,I类会议主要用于研发过程中,也是临床过程中的重大事件,对受试者和产品本身都可能带来巨大隐患和伤害。Ⅱ类会议贯穿整个产品临床研究以及批准上市后的风险控制。其他类型的问题沟通,则属于Ⅲ类会议。
同时《办法》还明确了申报时间以及申报资料要求和流程。Ⅰ类会议在提出会议申请后30天内召开;Ⅱ类会议在提出后60天内召开;Ⅲ类会议在提出申请后75天内召开。当然,审评中心在召开之前会和申办方提前沟通,如果沟通过程中已经把问题解决,会议可以取消。会后形成的会议纪要需要双方签字并且作为申报资料,也是审评依据。
可以说,新的《办法》让申请人有一个明确和规范的渠道,提供自己的诉求,也体现出药品审评中心对于申请人以及整个行业开放的态度。说明我国药品审评改革中公开透明的宗旨。
福建药监,厦门政府对万泰的重视度,你很难想象的。
三类会议没什么用哦,要一二类会议才是重点
三类会议是什么东西?
2024年能上市?估计是你出批文了
医生玩万泰水平真的高
这个什么情况,等于是9价HPV疫苗快上市了哦,
这是沟通九价男性临床的