
2023年6月2日/医麦客新闻 eMedClub News/--近日,Avidity Biosciences的科研人员在Nucleic Acids Research上发表文章“Targeted tissue delivery of RNA therapeutics using antibody–oligonucleotide conjugates(AOCs)”。文中展示了抗体-寡核苷酸偶联物(AOCs)在肝脏、非肝(肌肉、心脏)组织中的递送,证明了AOC具有良好的靶向性以及目的mRNA下调的功能性。

▲ 图片来源:NAR
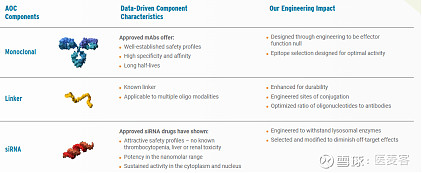
Avidity的AOC平台旨在将单克隆抗体(mAb)的成熟技术与寡核苷酸疗法的精确性和效力相结合,将寡核苷酸递送除肝脏以外的组织或细胞,为患者开辟新的潜在治疗方法。
▲ 图片来源:NAR
文章以抗体偶联siRNA出发,通过单抗靶向ASGR、TfR1受体,验证AOC在啮齿类动物中的组织靶向性,再到siRNA下调不同mRNA(MsTN、DMPK、Ssb)的程度,体现出AOC在体内良好的药理活性。同时在非人灵长类动物实验中表现出与啮齿类相当的效果。最后将寡核苷酸种类扩大到ASO及PMO,证明了AOC平台的适用性。

把握行业趋势,点击图片报名
AOC的靶向性
eMedClub
验证ASGR和TfR1靶向性
eMedClub
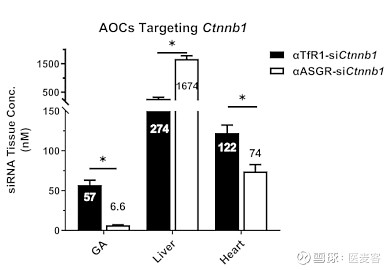
在小鼠实验中,研究人员将靶向cateninβ1(Ctnnβ1) mRNA的siRNA(称为:siCtnnβ1)偶联到抗ASGR或TfR1的抗体上,分别用于肝脏或骨骼肌的siRNA递送。
TfR1-siCtnnβ1与ASGR-siCtnnβ1在腓肠肌中siRNA浓度为9:1,在肝脏中为1:6。这些结果与TfR1在肌肉中的表达和ASGR主要在肝脏中的表达一致。并且心脏中TfR1-siCtnnβ1的siRNA浓度相比ASGR-siCtnnβ1增加1.5倍表明,表明TfR1靶向也可提供受体介导的心脏递送。
▲ 图片来源:NAR
进一步证明组织特异性
eMedClub
为进一步证明靶向TfR1的AOC的在肌肉中的特异性,研究人员设计了靶向Ssb mRNA(小RNA结合核酸外切酶保护因子)的siRNA(Ssb mRNA在各种组织中普遍表达)。结果表明,在腓肠肌中对降低Ssb mRNA的半数有效量为0.45nM。相比之下,在心脏中的效力低10倍,在肝脏中的效力低100倍。在其他组织(包括肾脏、脾脏和胃肠道)活性极低或无活性。

▲ 图片来源:NAR
AOC的药理活性
eMedClub
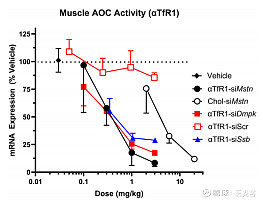
为了确定由靶向TfR1抗体递送到肌肉中的siRNA是否具有药理活性,在小鼠体内测试了靶向不同肌肉表达基因的siRNA,以靶向肌生长抑制素(Mstn)的siRNA为例,骨骼肌中Mstn的mRNA表达降低幅度>80%,呈剂量依赖性降低。此外,与胆固醇(Chol)配体与siRNA偶联相比,TfR1-siMstn的效力至少高10倍,表明AOC平台相对于非靶向配体的偶联具有更高的效率。
▲ 图片来源:NAR
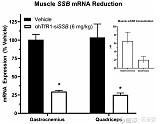
基于AOC平台在小鼠体内具有良好的药理活性,进一步在非人类灵长类动物(食蟹猴)中进行了测试,siRNA靶向猴Ssb mRNA,相较于对照,腓肠肌和股四头肌中Ssb mRNA表达减少75%。
▲ 图片来源:NAR
AOC平台的适用性
eMedClub
鉴于寡核苷酸治疗包含不同核酸种类,并利用多种药理作用机制,研究人员评估了AOC平台对其他化学类别的适用性,包括了PMO(外显子剪接开关)和硫代ASO(核糖核酸酶H1介导的mRNA降解)寡核苷酸。
将一个靶向DMPK mRNA(肌强直营养不良蛋白激酶)的ASO偶联至TfR1抗体(TfR1-asoDMPK),腓肠肌中DMPK mRNA减少75%。而未偶联的裸ASO需要增加25倍的剂量才能达到一样的活性,这进一步证实了受体介导递送的具有良好的药理活性。
文中还将靶向DMPK的ASO与siRNA进行比较,发现两者在同剂量下(5.4mg/kg)对腓肠肌中DMPK的效果相当。但与siRNA相比,肝脏中的ASO含量高达10倍,siRNA在肝脏中的含量可忽略不计。这些数据表明,非TfR1介导的机制可能是导致肝脏中ASO摄取的原因,而这种情况可能取决于所采用的寡核苷酸的种类。
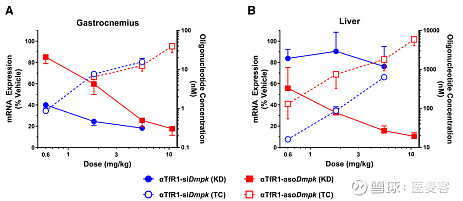
▲ 图片来源:NAR
AOC企业进展
抗体偶联寡核苷酸企业进展
eMedClub
eMedClub
Avidity在研管线中有三款药物披露了具体的适应症,包括1型强直性肌营养不良症(DM1),面肩肱肌营养不良症(FSHD),杜氏肌营养不良症(DMD),目前都处于临床1/2期阶段。此前由于严重不良事件报告,FDA对AOC-1001项目进行部分临床搁置,直到今年4月Avidity展示了该项目的积极数据,证明了多种临床结局指标、疾病改变以及良好的安全性和耐受性。在5月17日,FDA放宽了临床搁置,允许增加给药剂量和更多的受试者招募。

▲ 图片来源:Avidity
eMedClub
与Avidity的AOC结构不同,Dyne therapeutics的专有平台FORCE™是将Fab片段通过linker连接有效载荷。Dyne此前在ASGCT2023上展示了AOC药物DYNE-101(TfR1-asoDMPK)治疗DM1的临床前数据(目前在1/2期),实现了对中枢神经系统(CNS)的递送,并在DM1模型中实现了在脑中的药理作用。在5月25日,DYNE-101获得了EMA授予的孤儿药认定。

▲ 图片来源:Dyne
推荐阅读:抗体-寡核苷酸偶联物(AOC)新进展亮相ASGCT,聚焦严重肌肉疾病的治疗
推荐阅读:抗体-小核酸偶联药实现肌肉/CNS双重递送,为罕见肌肉疾病带来新希望
Tallac Therapeutics
eMedClub
Tallac的新型Toll样受体激动剂抗体偶联物(TRAAC)平台能够全身递送靶向TLR9激动剂(T-CpG)以进行免疫激活。在研的TAC-001(目前在1/2期)由CpG(寡脱氧核苷酸)与新型Nectin-4(肿瘤相关抗原)抗体偶联而成。正在进行的临床试验旨在评估静脉内给药TAC-001的安全性,药代动力学和初步抗肿瘤活性,预计将在2023年的医学会议上报告初步临床数据。
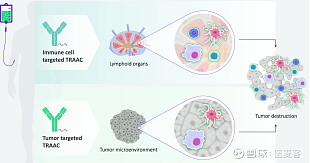
▲ 图片来源:Tallac
推荐阅读:万物皆可偶联,新型抗体寡核苷酸偶联物(AOC)完成首例给药
结语
eMedClub
Avidity此次发表在NAR上的临床前数据表明,TfR1受体介导的AOC具有良好的靶向性以及在肌肉组织中的药理活性。并且Dyne也发现靶向TfR1的抗体能够将寡核苷酸递送至中枢神经系统中。证明AOC在神经肌肉疾病中具有良好的发展前景,并且AOC疗法还可能扩展到肿瘤治疗领域。
参考资料:
1.网页链接
声明及版权说明
声明:本文旨在于传递行业发展信息、探究生物医药前沿进展。文章内容仅代表作者观点,并不代表医麦客立场,亦不构成任何价值判断、投资建议或医疗指导,如有需求请咨询专业人士投资或前往正规医院就诊。
版权说明:本文来自医麦客内容团队,欢迎个人转发至朋友圈,谢绝媒体或机构未经授权以任何形式转载至其他平台,转载授权请在文章下方留言获取。

点点“分享”、“点赞”和“在看”,给我充点儿电吧~