通过这篇文章,我们只能管中窥豹,了解一个可能是近代医学领域最重大的发现之一,它关系到人类很多“束手无策”的疾病,对于人类医学史来说它太新了。
上个世纪90年代初期,科学家发现了人体存在一个极其重要的生理系统——内源性的汉麻素类系统,其中研究最多的两种汉麻素受体是CB1和CB2。CB1 受体在中枢神经系统中占主导地位,而 CB2 受体则存在于免疫系统中。(全面剖析人体内源性汉麻素系统)
直到近几年,CB3才“显出真身”——CB3 受体以 GPR55 的名义隐藏了起来。医疗从业者对GPR55应该都不陌生,一旦其功能发生障碍后会出现各种疾病包括癌症。起初,科学家并不知道这种受体可以接受汉麻素。(更多资讯关注翰菩时代)
如今,对CB3受体的研究开辟了一个新的医学时代,很可能解开汉麻药物治疗疾病的未解之谜。下面我们来逐一探讨这个人类的“生命密码”——汉麻素受体CB3,它是否能带来巨大的医学进步?

先简要介绍ECS
内源性汉麻素系统 (ECS) 是一个调节情绪 、认知 、植物神经系统和运动过程的神经调控系统 ,对脊椎动物基本的生理和病理功能发挥重要作用 ,包括疼痛调节、免疫功能、保护神经、控制食欲以及治疗癌症和心血管疾病 等。
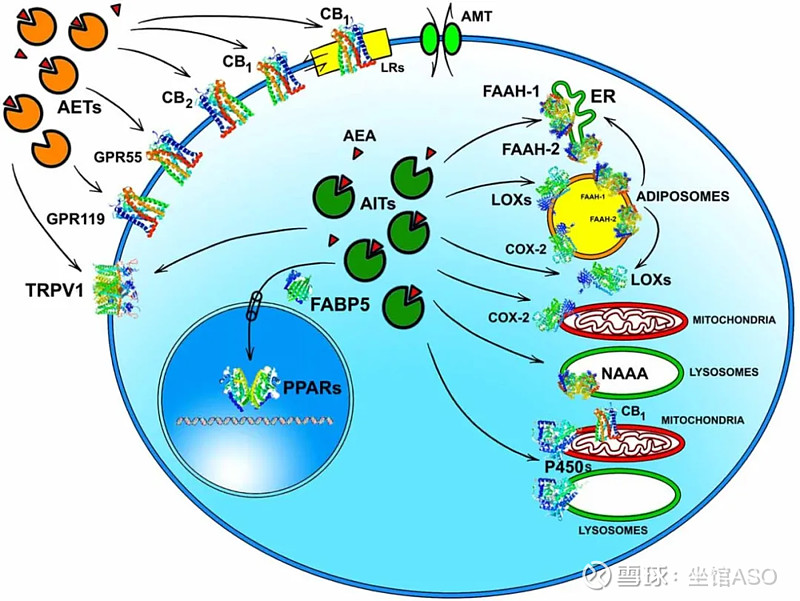
ECS包括汉麻素受体 (cannabinoid receptor,CB receptor)、内源性汉麻素 (eCB)以及合成和降解eCB的各种酶 。临床研究表明汉麻素受体可以作为治疗多种重大疾病的药物靶点 。
更多参考:
TED演讲—都2021年了,你却还对内源性汉麻素系统一无所知?
什么是GPR55受体?
1999年 ,科学家首次从人脑中分离和克隆出孤儿G蛋白偶联受体GPR55。孤儿受体这个名称意味着,科学还不知道是什么激活了这个受体。GPR55蛋白含有319个氨基酸 ,分子量为37kD,编码基因GPR55定位于染色体2q7上 。
GPR55受体在中枢神经系统中广泛分布,海马体、尾状核、下丘脑、小脑和脑桥等部位的神经元和神经胶质细胞中均高表达GPR55。外周组织如内皮细胞、肾上腺和胃肠道中也有GPR55分布。
现代医学研究显示, 高表达的GPR55在淋巴细胞和脾,以及多种肿瘤细胞中也有分布,并且与肿瘤的增殖速率呈正相关。简单理解就是控制GPR55受体就可能直接抑制肿瘤的增殖!
2012年,《Oncogene》杂志上的一则研究证实GPR55驱动小鼠皮肤肿瘤的发展。GPR55基因缺陷小鼠比野生型老鼠更能抵抗DMBA/TPA诱导的乳头状瘤的形成。GPR55的促肿瘤作用主要是由于其对癌细胞的增殖优势。
此外,GPR55能增强皮肤癌细胞的锚定独立生长、侵袭和体内致瘤能力,这表明它不仅促进肿瘤的发展,而且对肿瘤的侵袭也至关重要。最后研究还发现相比于健康组织,GPR55在人皮肤肿瘤和其他人鳞状细胞癌中都存在相应的表达上调。
这些研究结果表明GPR55在皮肤肿瘤的发生发展中具有至关重要的意义,这种受体可以作为一种新的生物标志物来诊断治疗鳞状细胞癌。(翰菩时代了解更多资讯)
2014年,East Anglia大学的研究团队解析了汉麻素THC(四氢汉麻酚)延缓肿瘤生长的分子机制,希望能够在此基础上合成具有抗癌能力的新药物。这项研究发表在《Journal of Biological Chemistry》杂志上。
研究人员发现,汉麻素受体CB2和GPR55在癌细胞中过表达,而且它们控制着癌细胞的命运。进一步研究表明,CB2和GPR55会形成异源二聚体,影响癌细胞的信号传导。CB2和GPR55的互作介导了THC的抗癌效果,这一发现将帮助人们进一步理解THC对肿瘤生长的具体影响。
除了THC,汉麻植物中的另一种主要成分,汉麻二酚 (cannabidiol,CBD)最早被发现对GPR55有拮抗作用。
为什么GPR55就是CB3受体?
汉麻素受体CB3一直不为科学家所知,因为它与其他汉麻素受体非常不同。尽管GPR55也能结合汉麻素配体,但其与典型汉麻素受体CB1和CB2的氨基酸序列同源性很低——只有 14% ,因此多年来寻找新汉麻素受体的科学家一直忽视它。
直到几年后真正的证据出现,2007 年发表在《英国药理学杂志》上的一项研究发现,包括CBD在内的几种汉麻素可能与GPR55结合。慢慢地,研究人员开始将GPR55视为真正的汉麻素受体。2008年发表在《PNAS》杂志上的一项研究,科学家才接受GPR55实际上就是CB3。
GPR55由植物汉麻素THC和CBD,以及低纳摩尔范围内的内源汉麻素anandamide,2-AG,诺拉丁醚激活。最近的研究表明溶血磷脂酰肌醇及其2-花生四烯酰基衍生物可能是GPR55的内源性配体。
因此 ,GPR55是一种明确区别于CB1和CB2受体新的非典型性汉麻素受体CB3,并且该受体似乎是与其他汉麻素受体一样的治疗炎症和疼痛的可能靶标。
我们直观地通过一项2019年的发明专利来参考GPR55在防治免疫系统疾病中的重要价值。
GPR55参与调节体内一系列生理、病理活动,包括中枢神经系统动作协调,神经或炎性疼痛,骨生理,胃肠道炎症,肥胖,2型糖尿病以及癌症等。GPR55已被提议作为治疗糖尿病,帕金森病,神经性疼痛和癌症的新潜在药物靶标。
释放CB3受体的医疗潜力
每一项新发现都让我们更深入地了解医用汉麻在体内的作用机制。汉麻素受体遍布全身,那么CB3藏在哪里呢?
CB3分散在全身,但集中在睾丸、脾脏和大脑中,也存在于小肠中。它在大脑的小脑区域最为密集,该区域控制身体的运动功能,例如行走和说话。
2008年的PNAS研究中,科学家们了解到了汉麻素与CB3相互作用时实际发生的情况。当THC进入体内并遇到CB3受体时,它会增加细胞内钙离子并抑制大脑中的M-current。从本质上讲,这意味着它可以控制神经元兴奋性,因此可用于维持健康的大脑功能。
CB3受体与癌症
基于这项研究,2017 年发表在癌症杂志《Oncotarget》上的一项研究表明,毫无疑问,GPR55表达与处于转移边缘的癌细胞密切相关。
科学家们认为,如果CB3受体可以被操纵——最有可能是通过植物汉麻素,就可能能够通过杀死它们的信号传递来阻止癌症的传播。换句话说,科学家们现在可能知道在哪里可以破译汉麻植物的潜在抗癌作用。
CB3受体与癫痫
长期以来,医用汉麻已被证明具有抗癫痫发作的特性。美国FDA批准的第一种基于汉麻素的药物目前用于治疗癫痫。仅仅几滴汉麻油,数十名癫痫患者的生活就发生了翻天覆地的变化。
但是,尽管有大量证据,但仍然没有令人满意的解释为什么汉麻具有如此强大的抗癫痫发作特性。将CB3受体集中在负责运动功能的大脑部分似乎是一个明智的答案。
2017年,一组发表在PNAS杂志上的科学家打破了这一概念。CBD 已经被证实可以降低 Dravet 综合征患者癫痫发作的频率和严重程度,这是一种罕见的儿童癫痫病。这项新研究进一步解释了它是如何工作的。
CB3与神经发育
在神经发育过程 中,轴突导向蛋白对神经网络的形成起重要作用 。有报道称 ,GPR55受体调控小鼠脊髓感觉特异神经元轴突排斥性导向过程。
在GPR55基因敲除的小鼠中,体内GPR55缺失会导致伤害感受神经元的轴突错误投射到本体感觉区域。这些研究表明GPR55可以调节神经系统发育过程中胶质细胞和神经元之间的信息交流 。
另有研究表明,GPR55在视网膜发育过程中表达,调节生长锥形态和轴突生长。这提示 GPR55在轴突生长和视神经支配中扮演重要角色,对视网膜一丘脑通路的正常发育起重 要作用 。
CB3与焦虑抑郁
目前关于GPR55在焦虑抑郁中的作用仍有争议。许多动物行为学结果显示 ,汉麻素CBD对不同模型均有抗焦虑作用 ,包 括高架十字迷宫、Vogel冲突实验和关联条件恐惧等 。
临床研究也显示,CBD能缓解大剂量THC所引起的焦虑样症状,还能减少人们在演讲或社交等紧张状态下的焦虑情绪。CBD除了拮抗GPR55之外,还能作用于CB1、CB2和PPAR7等受体。
CB3与疼痛
已知汉麻素类能通过作用于CB1和CB2抑制神经元兴奋性来发挥镇痛效应 ,但GPR55在其中扮演着怎样的角色呢?
大直径DRG神经元含有丰富的GPR55,其激活后 ,一方面增加Ca内流 ,另一方面通过 M一钾通道抑制K外向电流 ,从而引起神经元兴奋。这提示 GPR55可能参与疼痛的发生和发展 。
已有研究证实了GPR55在炎性痛和神经病理性痛中的作用。在炎性疼痛动物模型和神经病理性痛模型中 ,研究结果均表明GPR55具有促痛作用。然而仍然有一些问题还不明确 ,例如 GPR55是如何调控机械性痛觉过敏的?
CB3与突触可塑性
在脑高级功能 中,GPR55敲除后小鼠的情境恐惧记忆正常 ,但是运动协调能力受损 。激动背外侧纹状体内的GPR55有助于提高大鼠在T迷宫中空间辨别能力 ,相反地,拮抗 剂对其学习能力有所降低。
腹腔注射O-1602能降低吗啡引起的条件性位置偏爱,显示GPR55对成瘾有戒断作用 。这些结果都表明, GPR55参与脑高级功能 ,但还须进行全面细致的研究 。
CB3受体研究的下一步
CB3功能的多样性决定了其在不同组织中扮演着不同的角色,在中枢神经系统中更是如此。通过研究CB3与中枢神经系统的关系,包括与内源性汉麻素系统 、神经发育、焦虑抑郁和疼痛的作用关系 ,为相关领域的研究者提供一条新的思路 。
确认一种新型汉麻素受体,不仅对基于汉麻药物来说是个好消息,这对所有类型的药物都是好消息。随着科学家们对人类内源性汉麻素系统的范围和功能有了更好的了解,揭开CB3的神秘面纱的日子不远了。
汉麻植物存在于世上的终极使命,被人们真正认识的那天也不远了。
