
“华兴资本医疗与生命科技行业周报”定期发布,专注从资本角度解读一周数据,并提供最新行业观察。
医疗与生命科技是华兴资本多年来关注并深耕的领域,目前已为近200个融资及并购项目担任财务顾问。
医疗与生命科技行业创新不断涌现,已经发展成为最活跃的行业之一,华兴资本始终支持、陪伴这一领域创业企业成长,致力为行业带来理性专业的声音。
作者 | 华兴资本医疗与生命科技团队
关注华兴资本微信公众号(ID:iChinaRenaissance),后台点击“兴观点”-“行业观察”-“生命科技”,获取更多医疗与生命科技行业相关信息。

济因生物完成数千万元天使+轮融资
深圳市济因生物科技有限公司,完成数千万元天使+轮融资,由天创资本独家投资。本轮融资主要用于核心技术平台的优化升级以及体内CAR-T管线的临床阶段工作推进。
行业视角:
济因生物是一家致力于为肿瘤患者提供普惠性的通用细胞治疗药物的创新型公司,其体内CAR-T治疗药物已完成临床前研发,正在积极推进研究者发起的临床试验(IIT)。
专注新药靶点和药物发现的CRO企业爱思益普完成B++轮融资
北京爱思益普生物科技股份有限公司宣布于近日完成了B++轮融资。本轮融资由亦庄国投领投,现有股东雅惠投资继续增持股份。这是爱思益普自2023年8月完成近亿元融资后,再次快速获得资本市场的支持。本轮融资将支持爱思益普为海内外制药公司提供更领先、更优质的服务。
行业视角:
爱思益普是2010年闫励博士和李英骥博士回国后联合创立。经过十多年的创新研发,爱思益普已经从离子通道靶点药物筛选的初创公司,发展成为全球领先的基于新靶点的药物发现生物学CRO,聚焦于药物发现的新靶点、新方法、新技术,建立了靶点驱动的药物发现生物学一体化平台,服务了全球1,000多家新药研发企业,从分子、细胞、组织、器官、动物等多个维度建立了从药物靶点验证到体内药效学验证的全流程一体化服务平台,每年支持数十项研发项目进行IND申报。
全和诚完成超亿元Pre-B轮融资
近日,天津全和诚科技有限责任公司宣布成功完成超亿元Pre-B轮融资。本轮由聚能创投独家投资。新一轮融资将主要用于核酸药物、递送系统、体外诊断等生物技术化学原料及下游应用开发和商业化推广。
行业视角:
全和诚致力于成为生命科学企业最信赖的合作伙伴,始终坚持创新引领,积极推进政产学研深度融合,拓展了技术和产品两个边界,形成了高度相关的一体化业务模式。凭借多年的技术沉淀,全和诚各大技术平台在相应赛道均处于行业领先地位,先后搭建了合成技术通用平台、交叉技术应用平台、基因治疗递送平台、核酸药物发现平台、IVD技术服务平台、知识产权运营平台。
爱楷医疗完成数千万融资
上海爱楷医疗科技有限公司与山东莒县经济开发区管委会达成算力中心及精密电子医疗器械项目千万级投资协议。本轮投资将主要用于爱楷医疗数字神经电刺激治疗设备的量产,包括新产品研发、临床研究、注册申请、核心技术迭代及商业化拓展。
行业视角:
由海外归国专家创建于2018年,上海爱楷医疗科技有限公司是一家主要从事微介入数字神经电刺激治疗设备、数字疗法、医疗信息化、大数据应用及AI应用的研发型数字医疗科技公司。爱楷医疗专注于数字疗法、数字硬件医疗产品和AI疾病诊疗,同时拥有完善的全院信息化系统产品、紧密型医共体产品、互联网医院产品。
中景纬视获新一轮数千万元融资
致力于以“前沿科技开启人类视觉科学新纪元”的中景纬视(苏州)光学科技有限公司继2023年成功获得天使轮投资以后,于近日顺利完成数千万元Pre-A轮融资,由瑞华资本领投,泰煜投资、蜂巧资本跟投。本轮融资将助力中景纬视持续推进临床研究、市场推广、品牌建设及新技术研发,开发更多创新性眼健康产品,切实解决临床中未被满足的需求与痛点,引领眼健康消费新风潮。
行业视角:
中景纬视成立于2022年,创始人及核心团队在眼科领域深耕二十年,具有丰富的临床推广和品牌建设经验,曾在中国眼科临床领域成功实现了多个产品的商业化。在短短两年时间内将全球独创的STOP KIT™动态时空光学膜推进到了商业化阶段,这充分证明了创始团队出色的技术转化、商业化能力和务实的经营理念。
智愈医疗完成超6000万元Pre-A++轮融资
北京智愈医疗科技有限公司于近期正式完成Pre-A++轮超6,000万元人民币融资。此次融资由辰德资本领投,联想之星跟投,老股东顺为资本、礼来亚洲基金(LAV)、众海投资持续加注。智愈医疗成立三年来完成多轮融资,本轮超募融资所募集资金将用于核心产品metaFlow®️高能水射流自主执行手术机器人(水刀手术机器人)的临床试验,以及新产品管线研发布局。
行业视角:
成立于2021年的智愈医疗,是专注于手术机器人和智能诊疗设备的国家高新技术企业、北京市专精特新中小企业。公司重点布局微创泌尿外科手术、介入手术和经自然腔道手术的领先创新产品。
微远基因完成数亿元D+轮融资
近日,微远基因宣布成功完成数亿元人民币D+轮融资,由科泉基金领投,天心基金跟投。本轮募集资金将主要用于推动病原分子精准诊断产品的研发与IVD化,加速整体解决方案在全国顶级医疗机构的落地开展。同时,微远基因将新建先进的分子诊断试剂和仪器生产基地。
行业视角:
微远基因成立于2018年,专注于基因诊断领域与感染精准医疗,着力构建基于基因组学、影像组学与EMR大数据的感染性疾病AI诊断体系,为临床提供感染精准诊断综合解决方案。公司目前已建成超过10,000㎡的研发中心、医学检验实验室和体外诊断产品GMP生产基地,并在北京、上海、广州、郑州、成都等多地设有检测中心和分支机构。公司已累积了超过40万例的病原宏基因组学大样本数据,并参与了如新冠病毒等重大病原的早期发现鉴定工作。
深智透医完成B+轮近千万美金融资
5月13日消息,知名AI医学影像企业深智透医刚刚完成B+轮近千万美元融资,累计融资额超过五千万美元。本次投资方包括聚焦深科技的知名硅谷投资机构Fusion Fund等过往投资机构,也引入了扎根硅谷的新进美元基金嘉加资本(ENVISIONX Capital)、Bluerun Ventures、上海文周投资及其它亚太区域战略合作方。本次融资将用于加速全球商业落地及产品研发创新。深智透医有多条在研产品线,海外影像质控类AI产品SubtleReformat(国产产品名SupReformat)近日获美国FDA批准,正式开始AI临床落地。
行业视角:
深智透医已围绕前沿AI技术及生成式模型,开发了医学影像全模态的AI产品,加速MRI、PET等医学影像检查,实现连续三年业务额翻倍增长,预计年内全球业务营收过亿。
强生宣布将8.5亿美元全现金方式收购Proteolgoix
美国新泽西时间2024年5月16日讯,Proteologix Inc.,一家聚焦于精准免疫学(precision immunology)方向的非上市生物技术公司,宣布与强生公司达成最终协议:强生公司将以8.5亿美元全现金方式收购Proteologix,同时未来可能额外支付一定金额的里程碑付款。
行业视角:
Proteologix系一家位于美国的临床前阶段的生物新药公司,公司聚焦于精准免疫学(precision immunology)方向,致力于研发针对自身免疫和炎症性疾病的新一代多特异性抗体(multispecific antibody)疗法。公司团队具有全面、综合的药物发现与开发能力,以及诸多成功的创新药研发经验。


安徽医保局:试剂、耗材联合议价新模式
5月13日,安徽省医保局发布《关于进一步加强公立医疗机构医用耗材采购管理的实施意见(征求意见稿)》公开征求社会意见的公告。值得注意的是,安徽医保局首次提出联合议价模式,对国家、省际联盟、省级集中带量采购外的品种,鼓励以省级医院、紧密型城市医疗集团、紧密型县域医共体为采购联合体,组成采购联盟议价采购。

安进DLL3/CD3双抗获FDA批准上市
FDA批准BMS的CAR-T细胞疗法一项新适应症
百济神州「泽布替尼」新适应症获批上市
多款医疗器械产品获批上市

安进DLL3/CD3双抗获FDA批准上市
5月16日,安进宣布,FDA已经加速批准DLL3/CD3双抗Tarlatamab上市(商品名为Imdelltra),用于治疗铂类化疗期间或之后疾病进展的广泛期小细胞肺癌(ES-SCLC)。
信息来源:医药魔方
FDA批准BMS的CAR-T细胞疗法一项新适应症
5月15日,美国FDA加速批准BMS的CD19 CAR-T细胞疗法lisocabtagene maraleucel(liso-cel,Breyanzi)用于复发或难治性滤泡性淋巴瘤(FL)成人患者,这些患者先前接受过两种或两种以上的全身治疗。
信息来源:医药魔方
百济神州「泽布替尼」新适应症获批上市
5月13日,中国国家药监局(NMPA)官网最新公示,百济神州BTK抑制剂泽布替尼胶囊一项新适应症上市申请已获得批准。根据中国国家药监局药品审评中心(CDE)优先审评公示,该产品本次获批的适应症为:联合抗CD20单抗奥妥珠单抗,适用于既往接受过至少二线系统性治疗的复发或难治性(R/R)滤泡性淋巴瘤(FL)患者。针对该适应症,泽布替尼已经于今年3月获得美国FDA加速批准。
信息来源:医药观澜
多款医疗器械产品获批上市
2024年5月15日,国家药品监督管理局批准北京市春立正达医疗器械股份有限公司的膝关节置换手术导航系统上市,型号为黄河INS 1-手持骨科机器人。
信息来源:器械之家
总部位于圣地亚哥的医疗器械公司Atraverse Medical近日宣布其HOTWIRE™射频(RF)导丝获得FDA批准。
信息来源:CCI心血管医生创新俱乐部
近日,RapidAI 宣布美国食品和药物管理局(FDA)已授予其 AngioFlow by RapidAI解决方案的510(k)许可。
信息来源:CCI心血管医生创新俱乐部
近日,蓝帆医疗股份有限公司发布公告称:中国国家药品监督管理局(NMPA)批准了子公司上海蓝帆博元医疗科技有限公司研发、生产的“心启™冠状动脉球囊扩张导管”产品注册申请,注册证编号为“国械注准20243030845”。
信息来源:器械之家
上海三友医疗器械股份有限公司发布了关于控股公司Implanet脊柱内固定系统获得美国FDA510(K)认证的自愿披露公告。
信息来源:思宇MedTech

穿越血脑屏障小分子获FDA授予突破性疗法认定
拜耳first in class产品两项III期研究数据公布,拟申报上市
礼来超长效胰岛素两项3期试验达主要终点
君实生物公布抗PCSK9单抗3期数据
晕车新药第二项III期研究成功,年内申报上市
近90%患者肿瘤缩小,创新细胞疗法2/3期试验即将启动
Merus:EGFR/LGR5双抗获FDA突破疗法认证,治疗头颈癌
诺和诺德血友病双抗III期研究成功,年内申报上市

穿越血脑屏障小分子获FDA授予突破性疗法认定
日前,Nuvalent公司宣布,美国FDA已授予其在研脑渗透性ALK抑制剂NVL-655突破性疗法认定(BTD),用于治疗先前接受过两种或两种以上ALK酪氨酸激酶抑制剂(TKI)治疗的局部晚期或转移性ALK阳性非小细胞肺癌(NSCLC)患者。
信息来源:药明康德
拜耳first in class产品两项III期研究数据公布,拟申报上市
5月16日,拜耳公布了Elinzanetant治疗中重度血管舒缩症状(VMS,旧称为潮热)的两项III期研究(OASIS 1和OASIS 2)数据。基于此积极数据,拜耳计划向监管机构提交Elinzanetant的上市申请。
信息来源:医药魔方Info
礼来超长效胰岛素两项3期试验达主要终点
礼来(Eli Lilly and Company)公布其3期临床试验QWINT-2和QWINT-4的积极结果,这些试验评估其在研一周一次胰岛素efsitora alfa(efsitora)在未曾接受过胰岛素治疗和需要每日多次胰岛素注射的2型糖尿病成人患者中的作用。分析显示,两项试验皆达成主要终点。与全球常用的每日基础胰岛素相比,efsitora降低患者糖化血红蛋白水平(HbA1c)的效果显示出非劣效性。
信息来源:药明康德
君实生物公布抗PCSK9单抗3期数据
5月17日,君实生物公布了该公司研发的重组人源化抗PCSK9单抗昂戈瑞西单抗治疗原发性高胆固醇血症和混合型高脂血症的3期临床研究数据,该项研究数据发表在了国际学术期刊《营养代谢与心血管疾病杂志》(Nutrition Metabolism And Cardiovascular Diseases,NMCD)。在该研究中,昂戈瑞西单抗表现出相当的显著降脂作用,患者每2周接受一次治疗,12周时低密度脂蛋白胆固醇(LDL-C,即“坏胆固醇”)水平显著降低70%以上。
信息来源:医药观澜
晕车新药第二项III期研究成功,年内申报上市
5月15日,Vanda Pharmaceuticals宣布其在研新药Tradipitant(曲地匹坦)治疗晕动症(尤指晕车)的第二项III期研究(Motion Serifos)取得了积极结果。基于两项III期研究的数据,Vanda将在今年Q4提交Tradipitant治疗晕动症的上市申请。
信息来源:医药魔方Info
近90%患者肿瘤缩小,创新细胞疗法2/3期试验即将启动
Immatics公司在其2024年第一季度的财务报告上公布其在研T细胞受体T细胞(TCR-T)疗法IMA203用以治疗经治转移性黑色素瘤患者的最新数据。分析显示,87%的患者实现肿瘤缩小,患者的确认客观缓解率(cORR)达55%。Immatics计划在2024年下半年的医学会议上,提供IMA203的下一次临床数据更新。同时,该公司亦计划在与美国FDA进一步讨论后,于今年启动IMA203作为二线及以上疗法,治疗黑色素瘤患者的注册性2/3期临床试验。
信息来源:药明康德
Merus:EGFR/LGR5双抗获FDA突破疗法认证,治疗头颈癌
2024年5月13日,Merus宣布Petosemtamab被FDA授予突破疗法认证,用于治疗复发性或转移性头颈癌。Petosemtamab为一款EGFR/LGR5双抗,为Merus的核心管线之一,头颈癌三期临床预计今年中启动。
信息来源:医药笔记
诺和诺德血友病双抗III期研究成功,年内申报上市
5月13日,诺和诺德宣布Mim8(NNC0365-3769/denecimig)治疗血友病A的IIIa期FRONTIER 2研究达到了主要终点。基于该积极结果,诺和诺德将在今年内提交Mim8的上市申请。
信息来源:医药魔方Info

嘉越医药3.45亿美元授出泛RAS抑制剂相关权益
超60亿美元,恒瑞医药授出GLP-1产品组合大中华区外权益
20亿美元:艾伯维与Gilagamesh合作开发新一代精神疾病新药
超20亿美元,武田引进一款抗Aβ疫苗
超10亿美元,赛诺菲引进一款p38α/β抑制剂

嘉越医药3.45亿美元授出泛RAS抑制剂相关权益
5月17日,嘉越医药与美国Erasca公司共同宣布签署一项全球独家授权协议。根据协议条款,ERASCA公司将获得Pan-RAS(ON)抑制剂JYP0015中国内地和香港、澳门地区之外的全球独家研究、开发和商业化的授权许可。嘉越医药将有资格获得首付及潜在近期付款高达2,000万美元,总计最高达3.45亿美元的潜在开发、商业化里程碑及全球行使权付款等,以及净销售额的分级特许权使用费。
信息来源:医药观澜
超60亿美元,恒瑞医药授出GLP-1产品组合大中华区外权益
5月16日晚间,恒瑞医药发布公告称将其自主研发的GLP-1产品组合有偿许可给美国Hercules公司,美国Hercules公司将获得在除大中华区以外的全球范围内开发、生产和商业化GLP-1产品组合的独家权利。作为对外许可交易对价一部分,恒瑞医药将取得美国Hercules公司19.9%的股权,且将从美国Hercules公司获得GLP-1产品组合授权许可费。此外,根据公告,这项合作的首付款和各项里程碑付款最高超过60亿美元。
信息来源:医药观澜
20亿美元:艾伯维与Gilagamesh合作开发新一代精神疾病新药
2024年5月13日,艾伯维与Gilgamesh Pharmaceuticals达成合作协议,利用后者在新型神经功能重塑因子(neuroplastogens)的创新平台,共同开发新一代精神疾病药物。根据协议,艾伯维支付6,500万美元预付款,19.5亿美元里程碑金额,以及中个位数到低十位数的销售分成。
信息来源:医药笔记
超20亿美元,武田引进一款抗Aβ疫苗
5月13日,武田宣布与AC Immune就针对Aβ的疫苗产品ACI-24.060达成了一项全球独家选择权和许可协议。该消息公布后,AC Immune的股价大涨33%。
信息来源:医药魔方
超10亿美元,赛诺菲引进一款p38α/β抑制剂
5月13日,Fulcrum Therapeutics宣布与赛诺菲就Losmapimod(洛吡莫德)的开发和商业化权益达成授权合作协议。根据协议条款,Fulcrum将获得8,000万美元首付款,并有资格在达到特定的监管和销售里程碑后获得高达9.75亿美元的额外付款,以及从Losmapimod在美国以外的年度净销售额中获得从低十位数开始递增的分层特许权使用费。赛诺菲将与Fulcrum在全球范围内合作开发Losmapimod并平分其全球开发成本。此外,赛诺菲将获得该药物在美国以外的独家商业化权益。
信息来源:医药魔方

募资7.2亿,健尔康IPO最新进展
2024年5月13日,上交所官网显示,健尔康医疗科技股份有限公司提交注册,保荐机构为中信建投,拟募集资金7.2亿元。
信息来源:思宇MedTech
“县城影像之王”再次冲击IPO
5月13日,港交所官网披露了江西一脉阳光集团股份有限公司在港交所提交的上市申请,公司上市材料被正式受理,独家保荐人为中信证券。
信息来源:器械之家

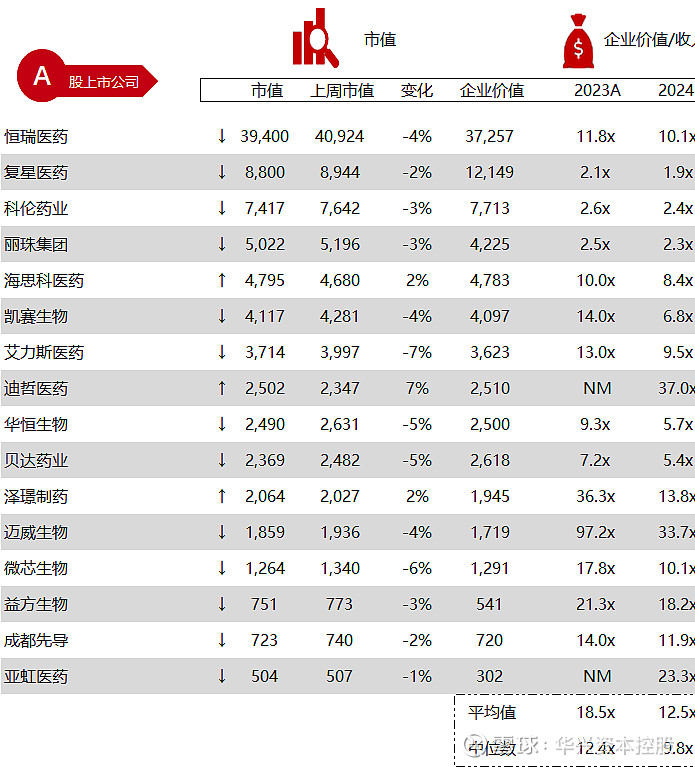
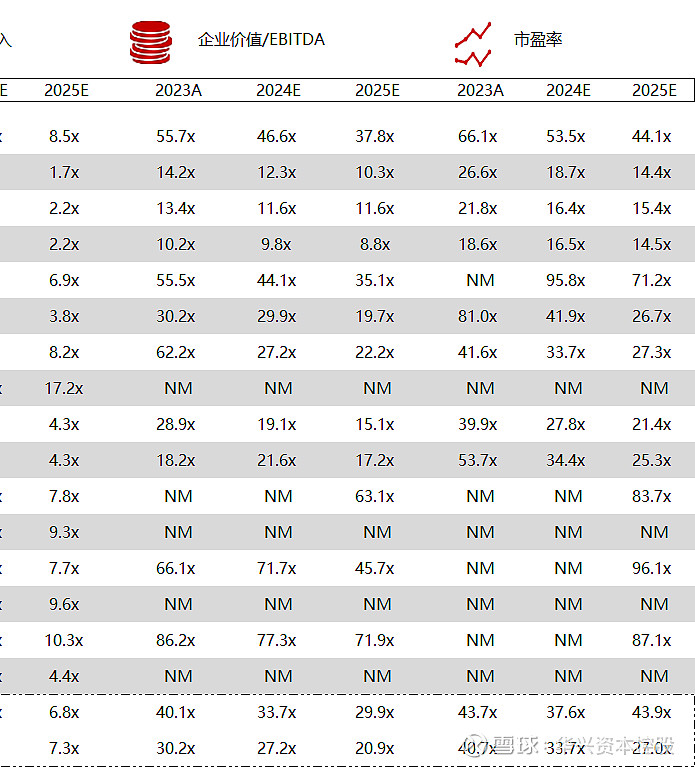
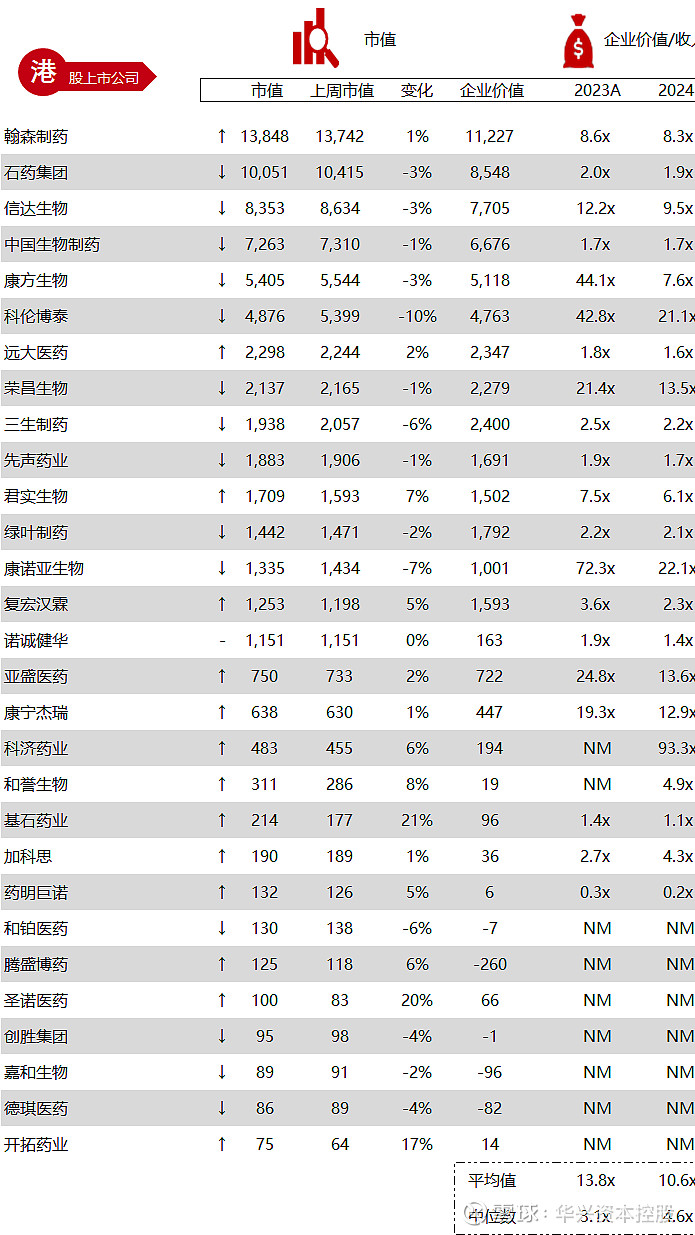
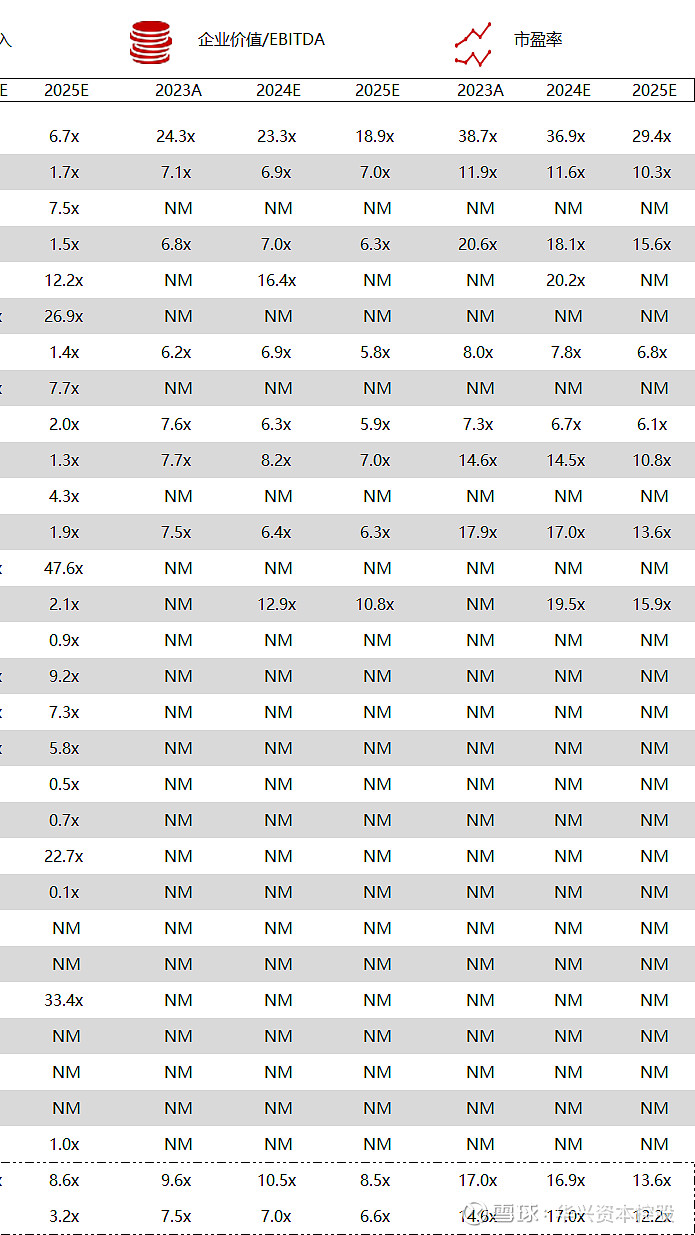
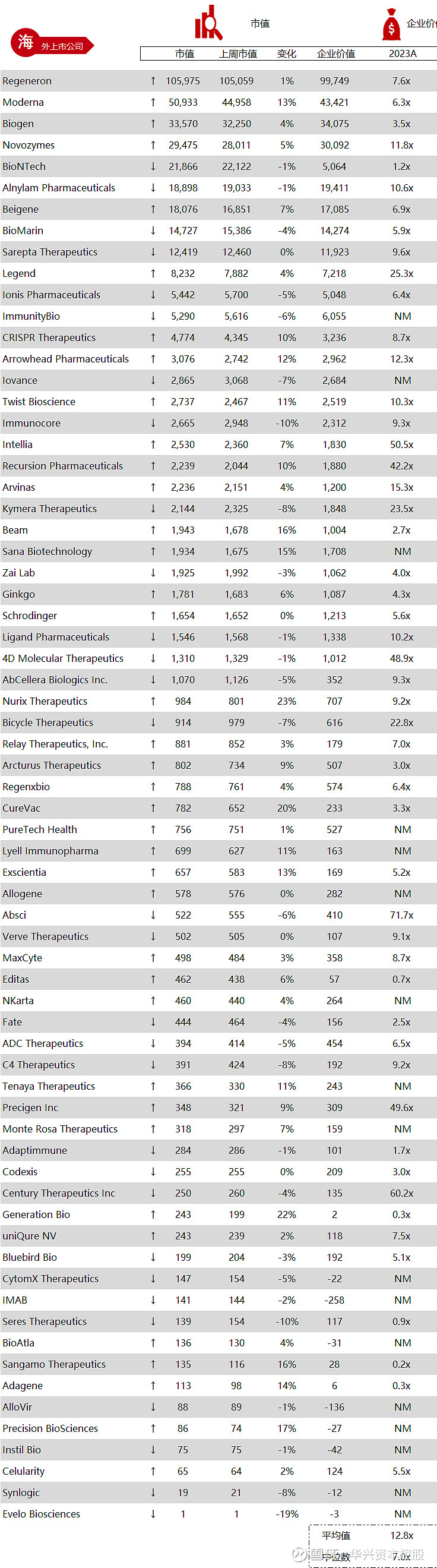
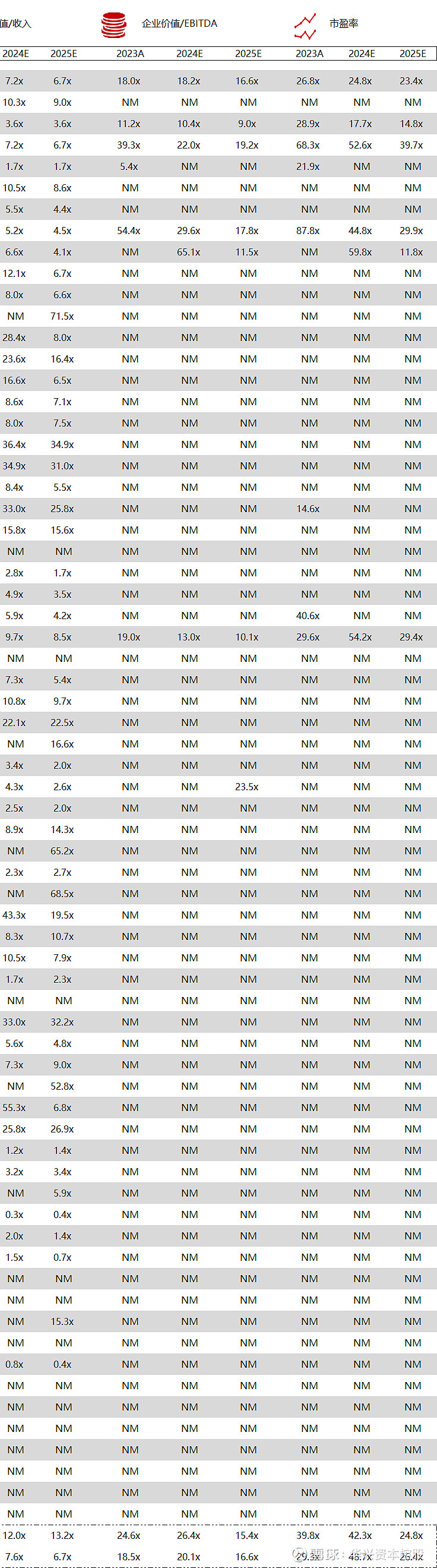
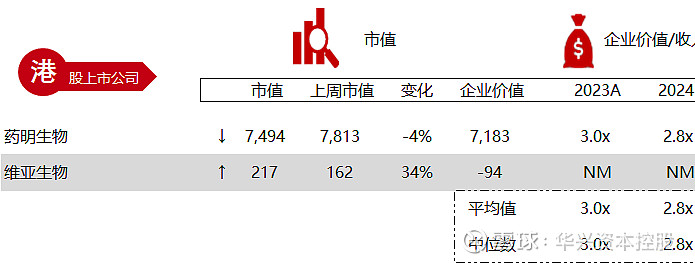
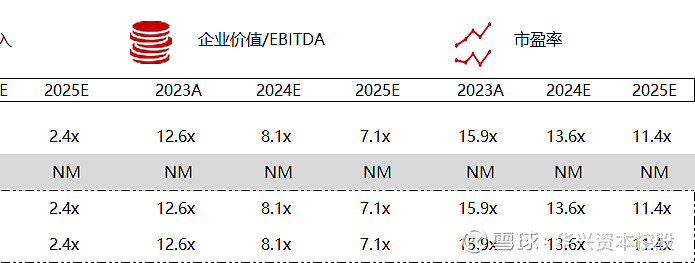
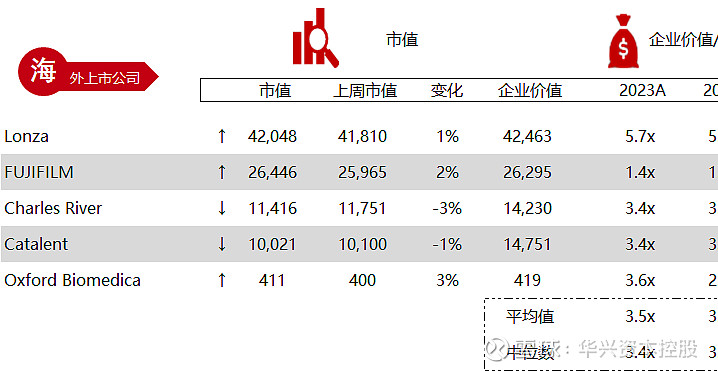
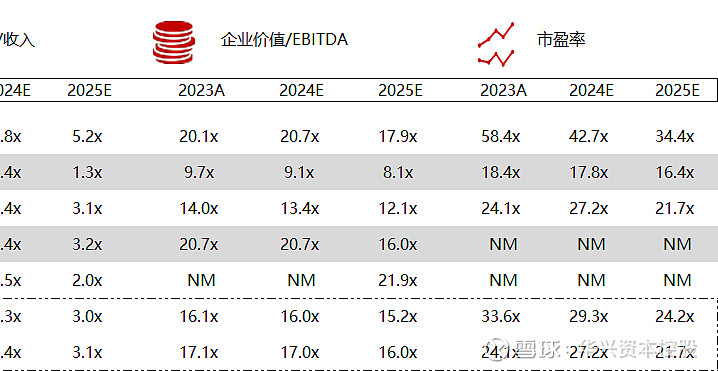
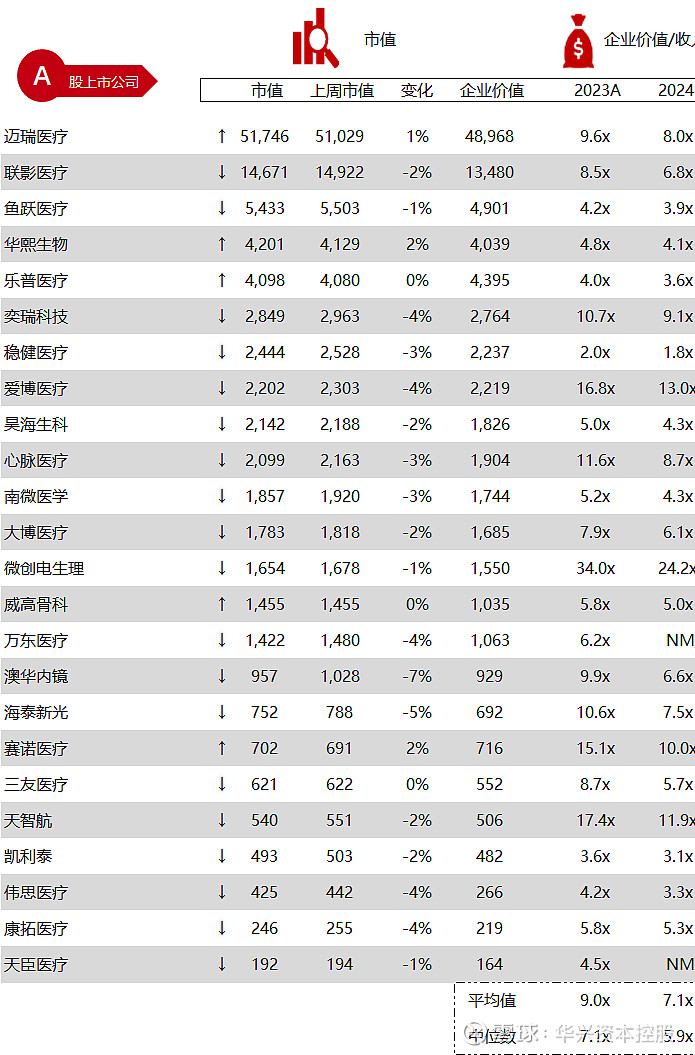
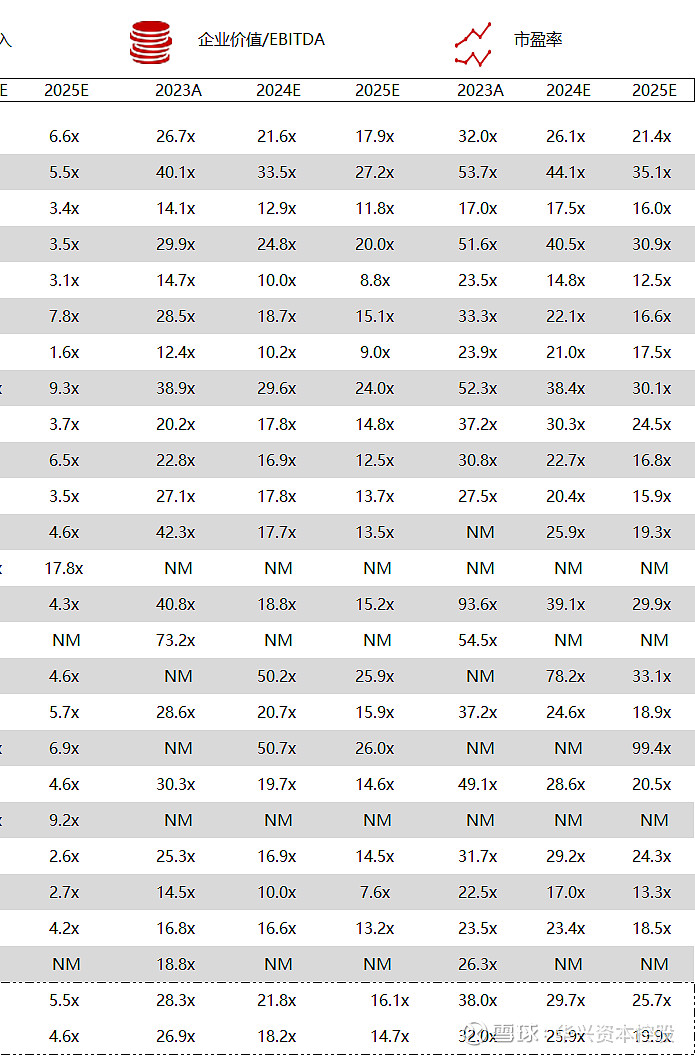
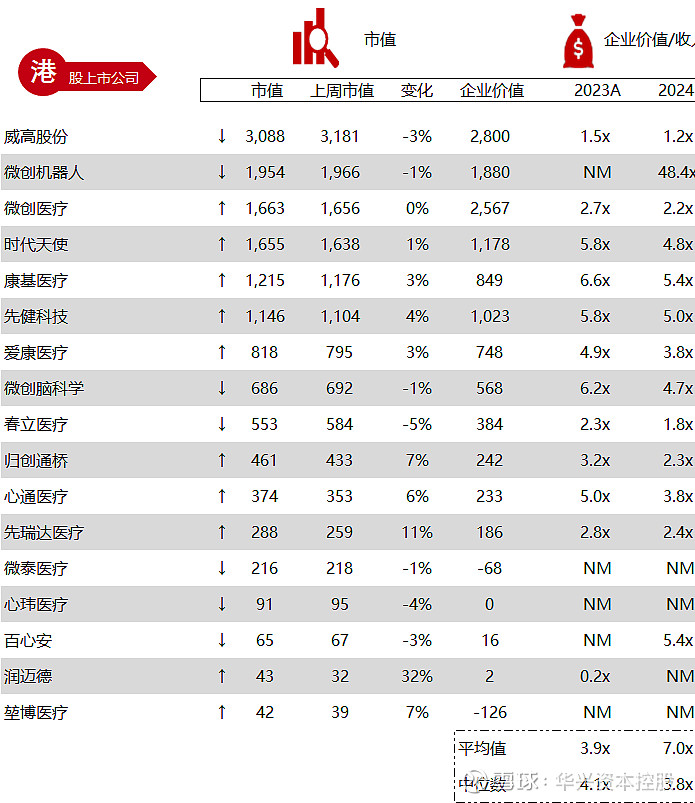
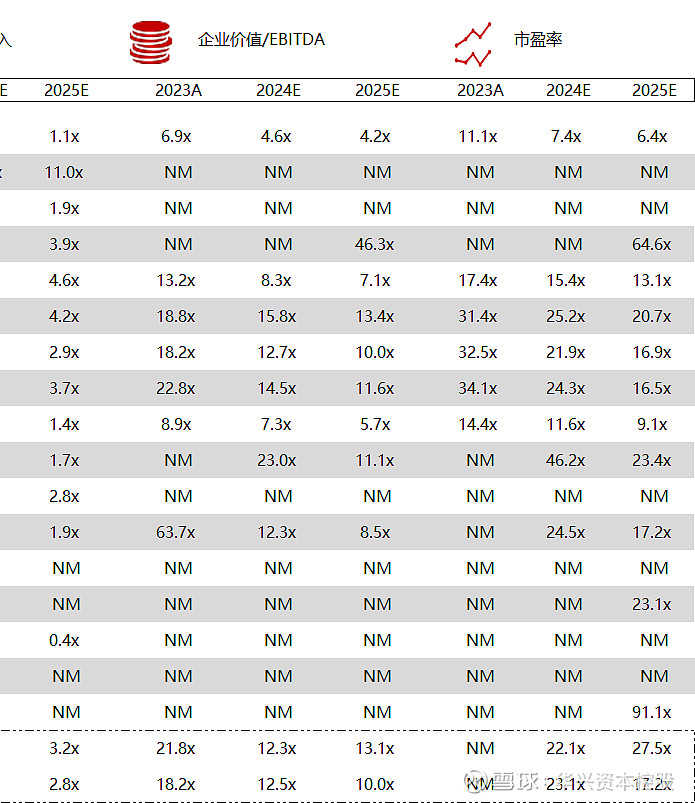
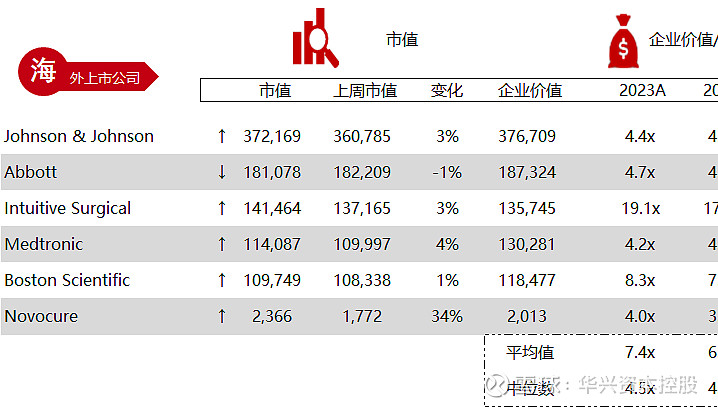
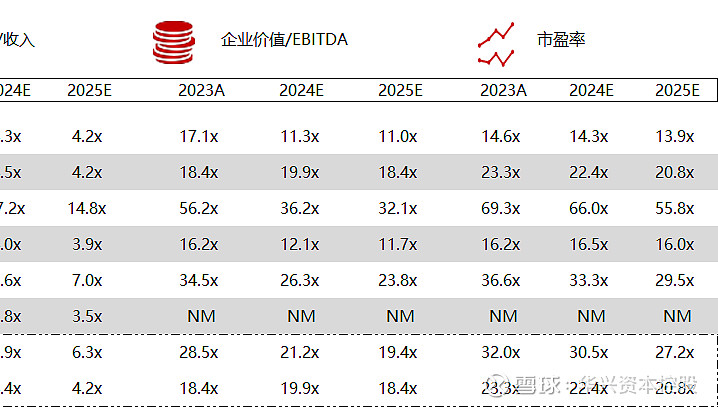
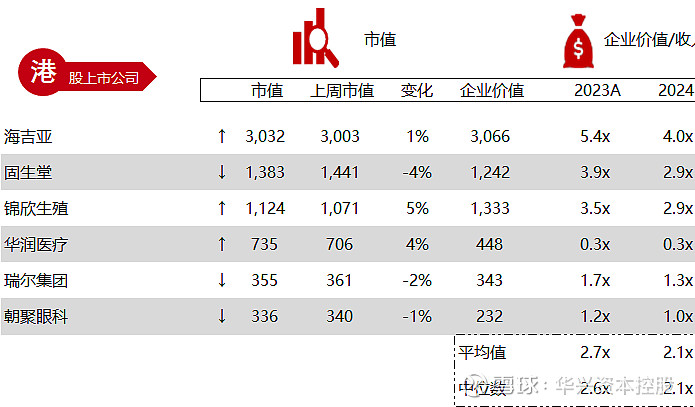
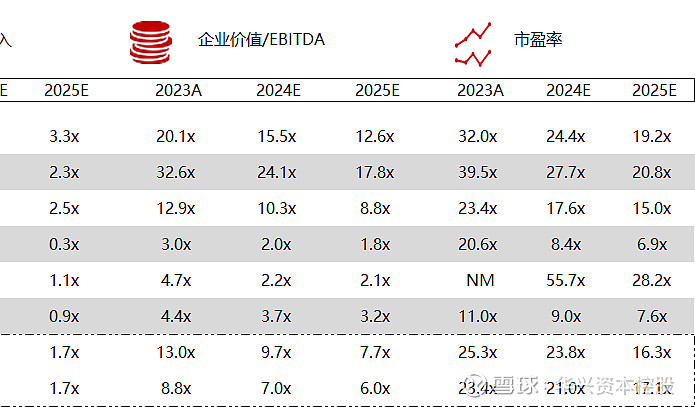
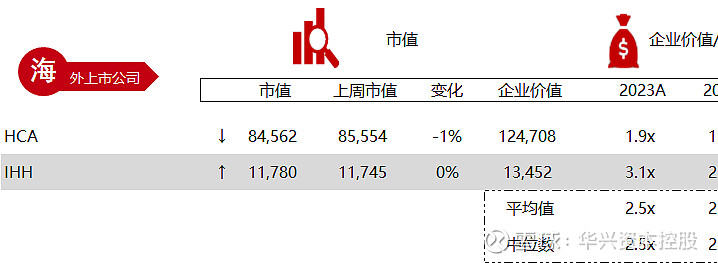
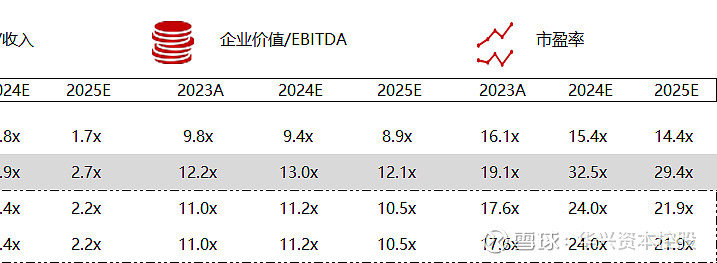
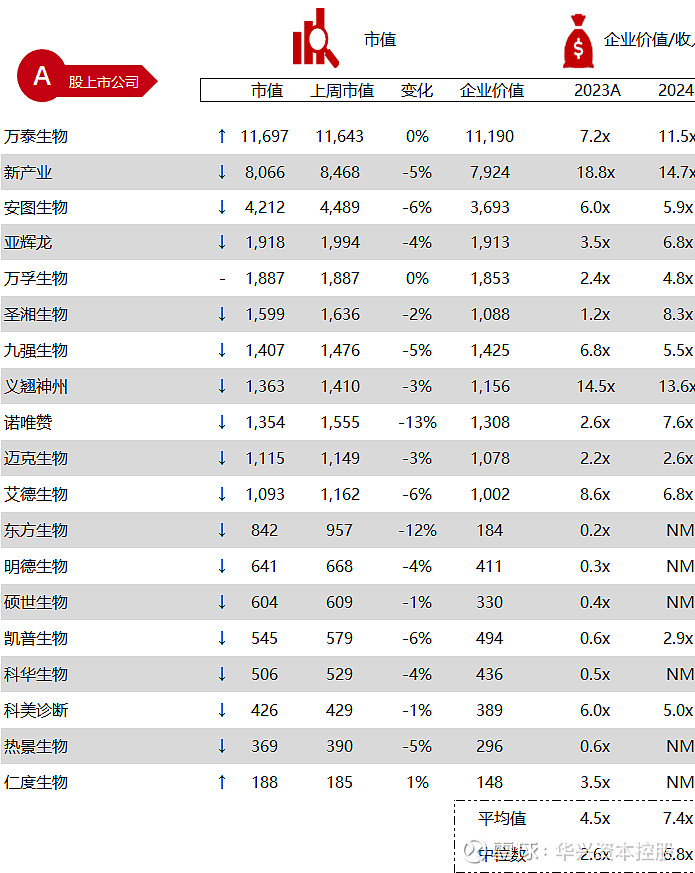
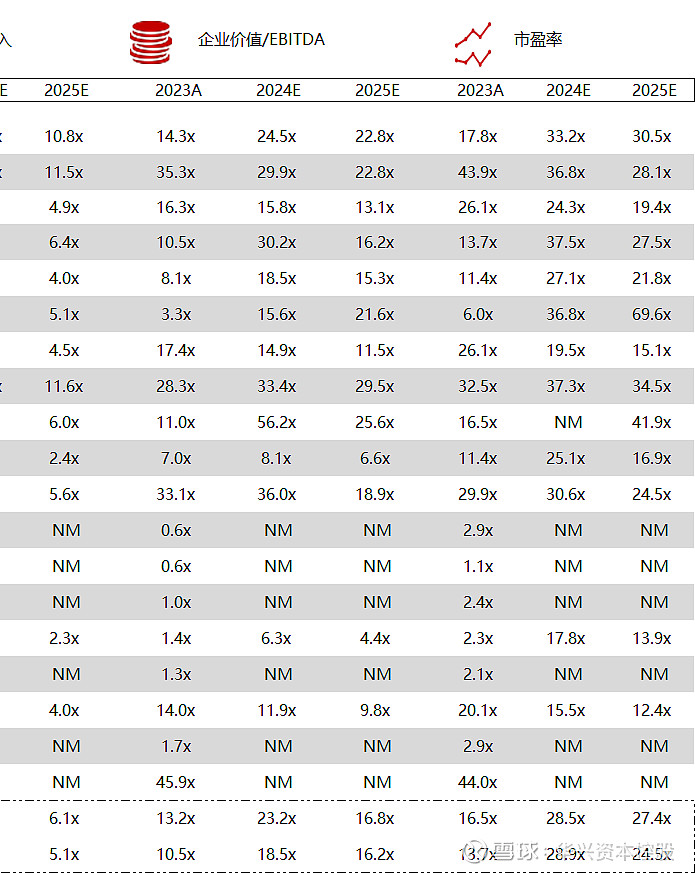
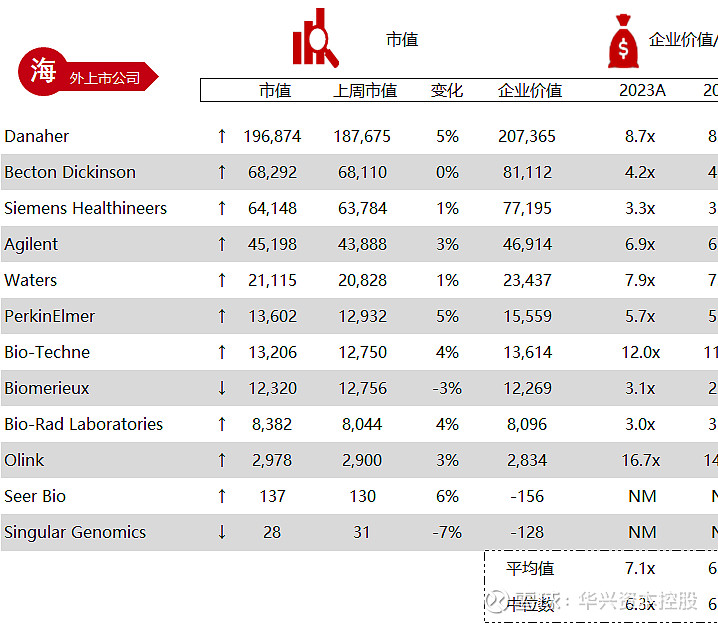
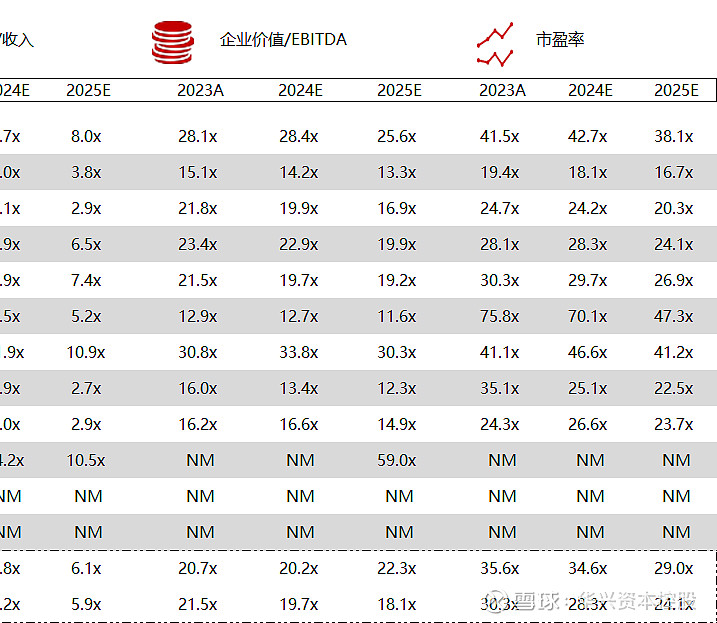
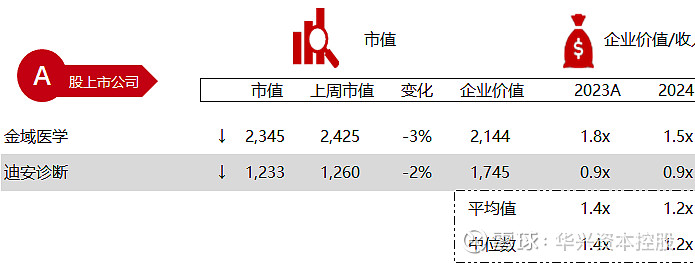
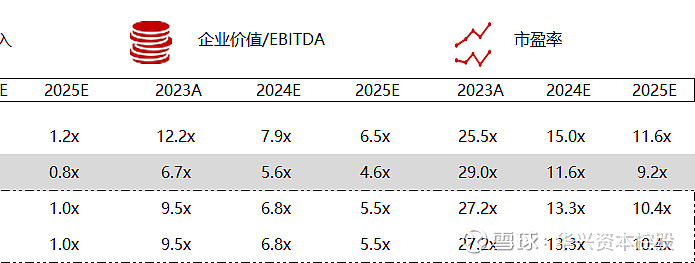
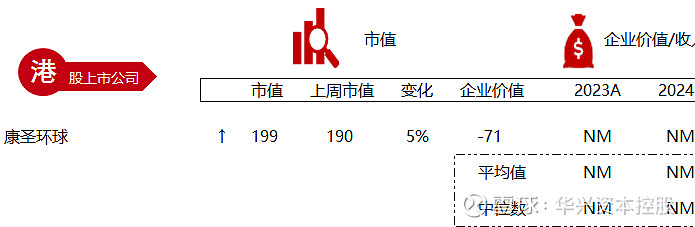
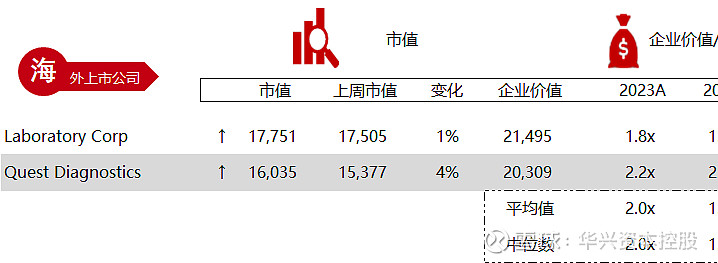
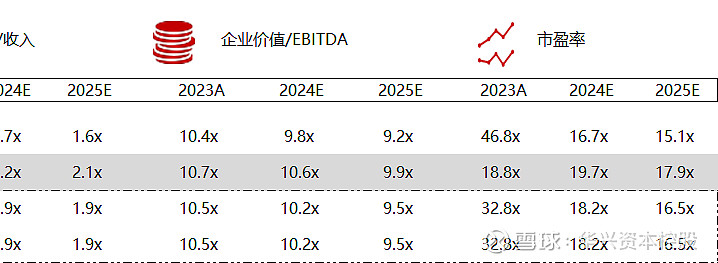
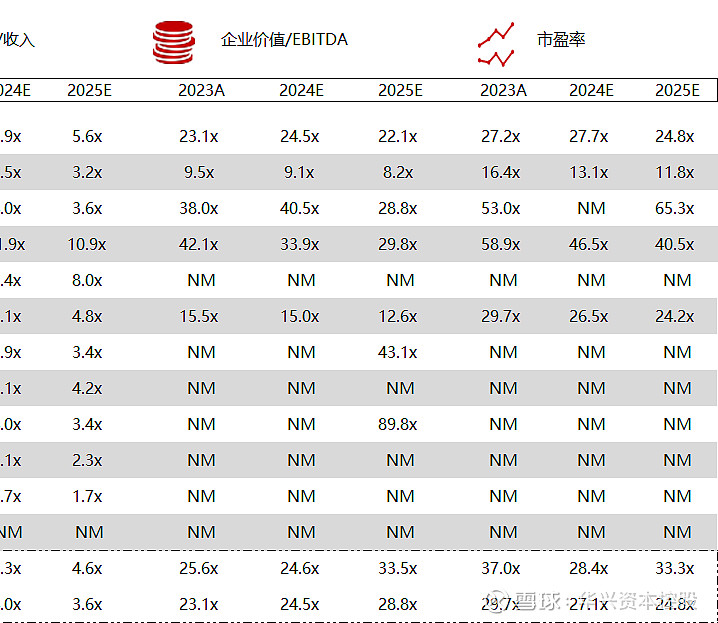
统计区间:2024年5月13日-5月17日

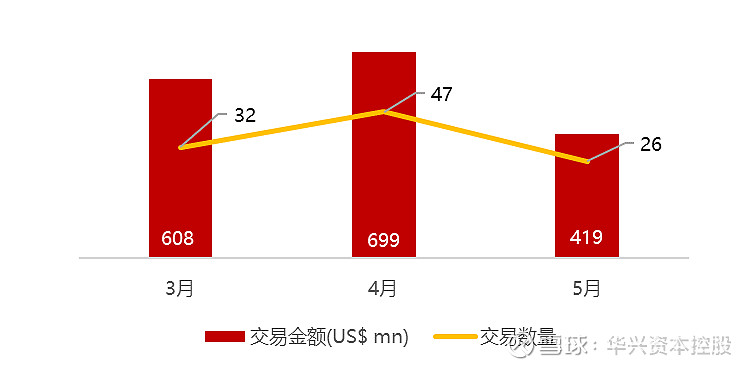



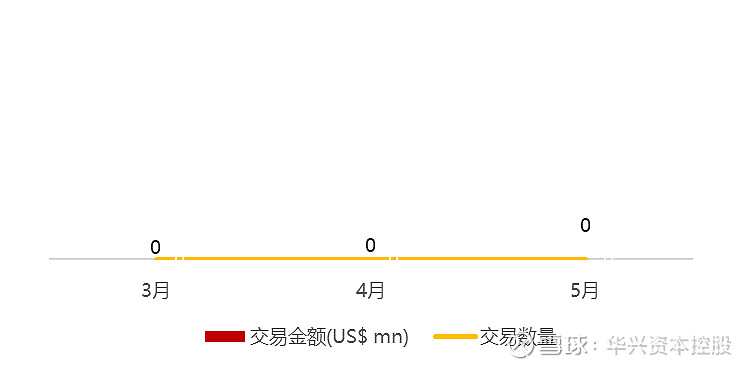

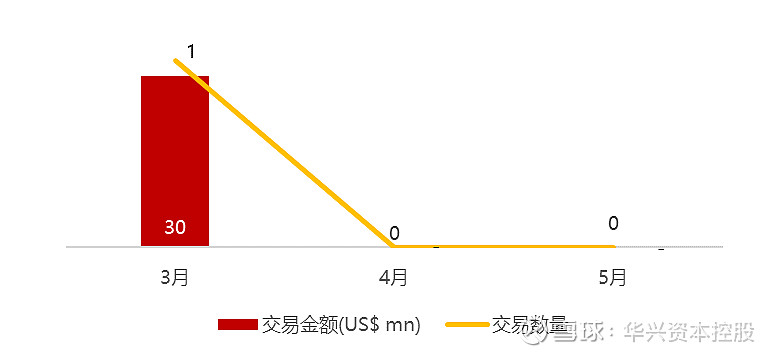

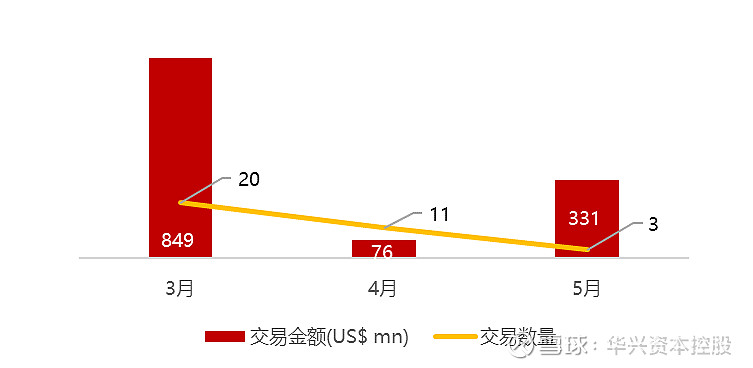





*数据来源:华兴资本内部整理

市值日期:2024年5月17日
市值单位:百万美元

>

>

>

>

>

>


>



>
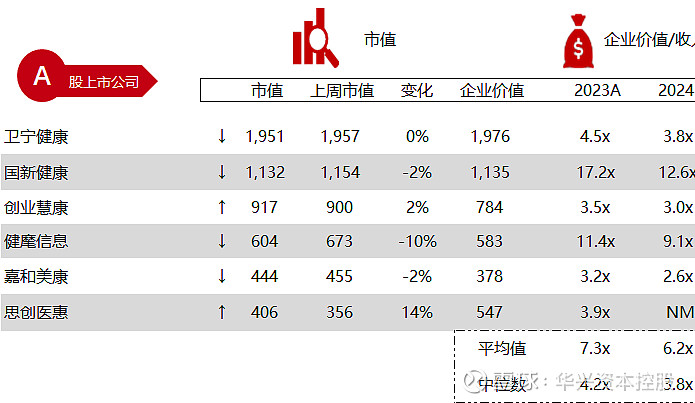
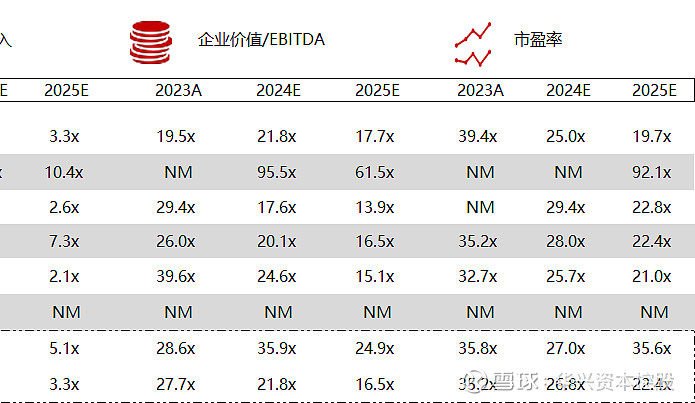
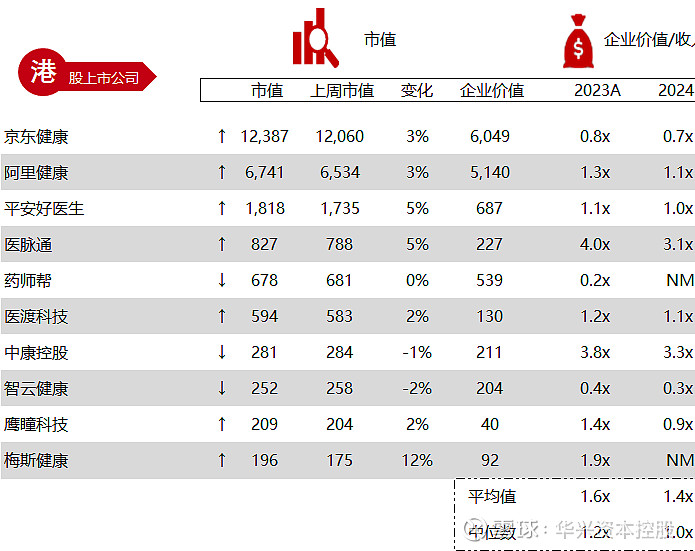
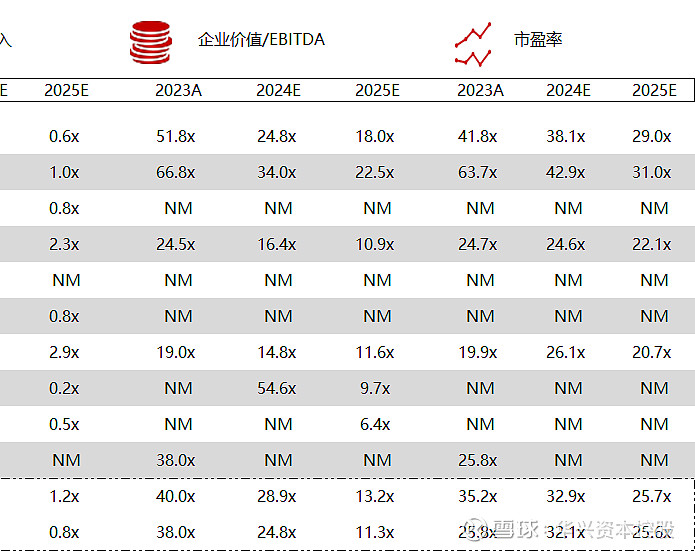
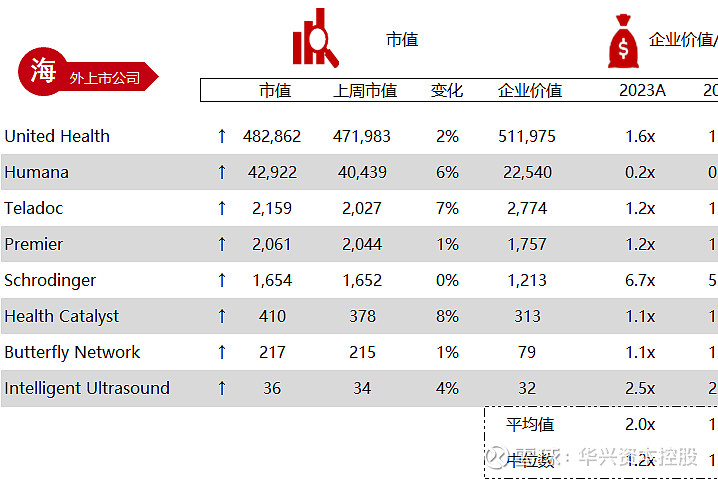
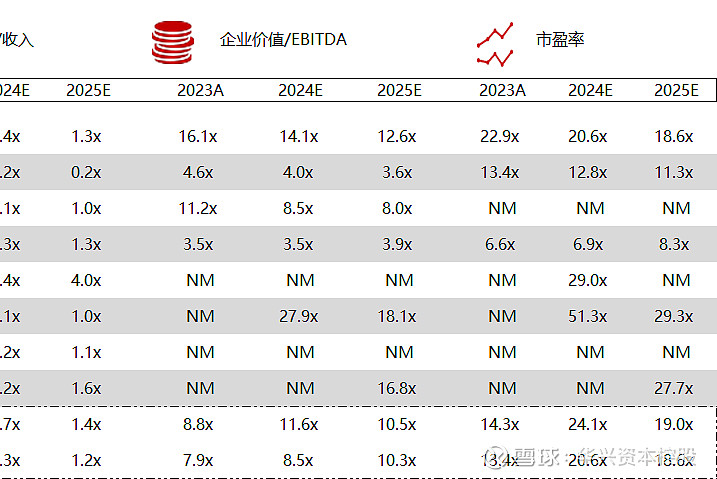
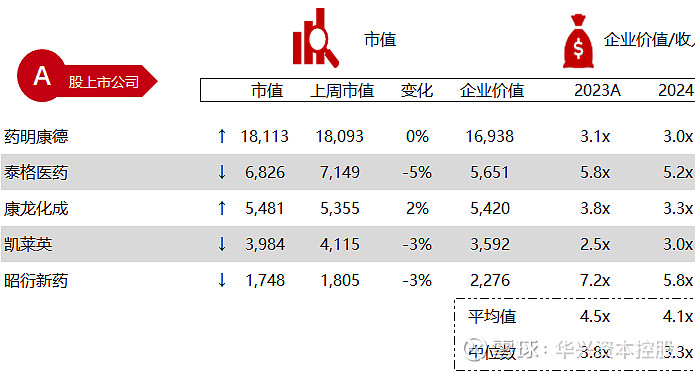
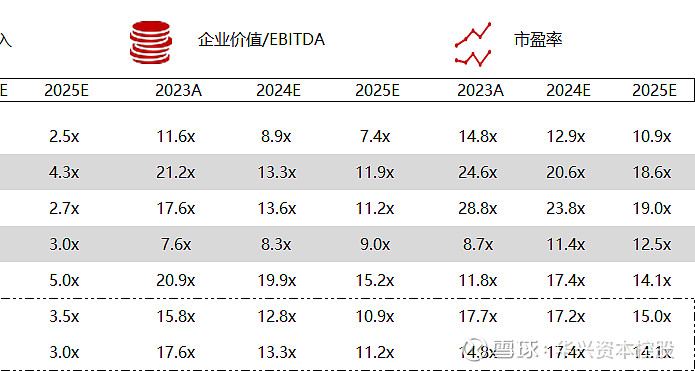
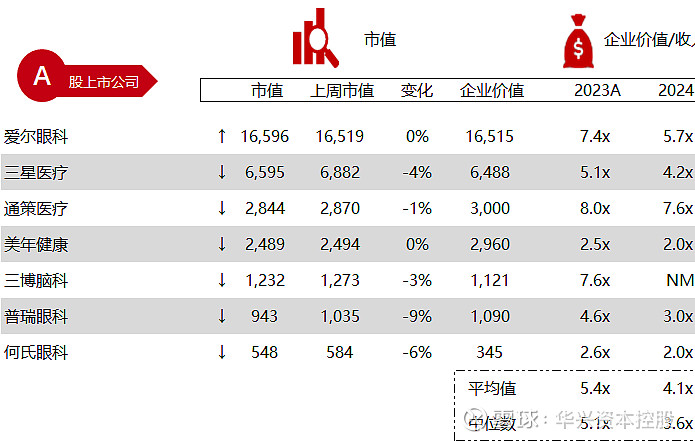
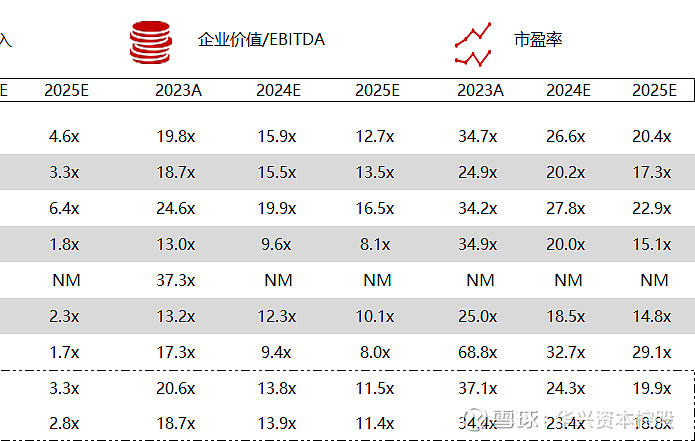
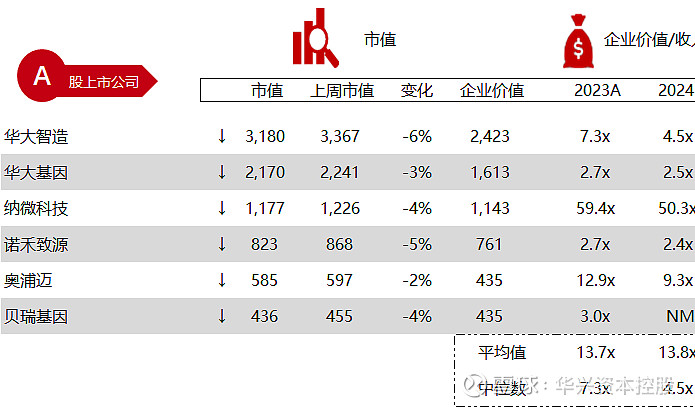
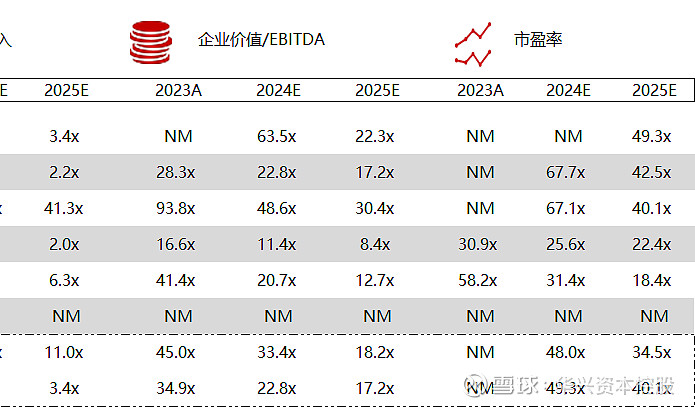
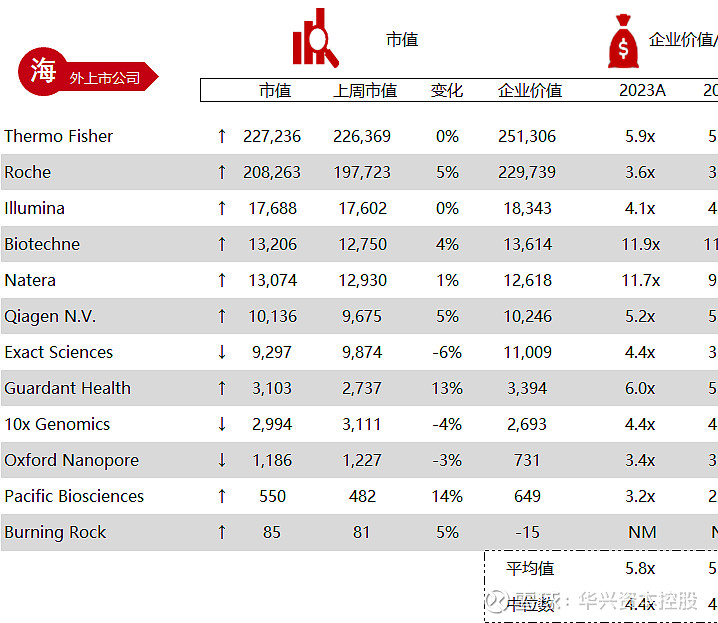
*数据来源:Capital IQ、招股说明书、研报、公司年报
免责声明:本文由华兴资本集团(连同其关联公司,统称“华兴资本”)编写,谨供接收方作参考用途,并非作为也不应被视为在任何地区对任何证券的研究报告,不构成买卖、认购证券或其它金融工具及产品的邀请或保证。本文所提及的上市公司仅为示例,不代表任何投资分析或投资建议。接收方不应仅依靠本文、而应按照自己的判断作出投资决定,并在作出任何投资行动前,咨询专业意见。
本文所载资料的来源皆被华兴资本认为可靠,但华兴资本概不担保本文所含信息的准确性、完整性或新近度。本文所载的见解、分析、预测、推断和期望均截至本文的发表日期,且可能在未经事先通知的情况下调整。华兴资本与本文所提及的公司之间可能存在或寻求业务关系,因此,接收方请知悉可能存在的影响本文客观性的利益冲突。华兴资本不对因使用本文而承受的直接或间接损失承担任何责任。本文受到版权和资料全面保护。